Mục lục bài viết
1. Giới thiệu
Hội chứng tĩnh mạch chủ trên (SVC syndrome) bao gồm một loạt các dấu hiệu và triệu chứng lâm sàng do tắc nghẽn dòng máu qua SVC (superior vena cava), có thể dẫn đến bệnh tật và tử vong đáng kể. Bệnh ác tính (malignancy) là nguyên nhân phổ biến nhất gây tắc nghẽn SVC, chiếm khoảng 70% các trường hợp. Tuy nhiên, gần đây tỷ lệ mắc hội chứng SVC liên quan đến catheter tĩnh mạch trung tâm và máy tạo nhịp tim (pacemaker lead) hoặc máy khử rung tim (defibrillator lead) đang gia tăng. Việc quản lý hội chứng SVC đang càng được quan tâm. Trước đây, xạ trị (radiation therapy) được coi là phương pháp điều trị đầu tay, đặc biệt ở những bệnh nhân bị tắc nghẽn đường thở. Tuy nhiên, trong những năm gần đây, liệu pháp nội mạch (endovascular therapy) thường được sử dụng trước tiên, hoặc kết hợp với xạ trị, để làm giảm nhanh các triệu chứng lâm sàng và giảm biến chứng.
2. Giải phẫu của SVC
SVC được hình thành từ sự kết hợp của các tĩnh mạch cánh tay phải và trái, cung cấp hệ thống dẫn lưu tĩnh mạch của đầu, cổ và chi trên.
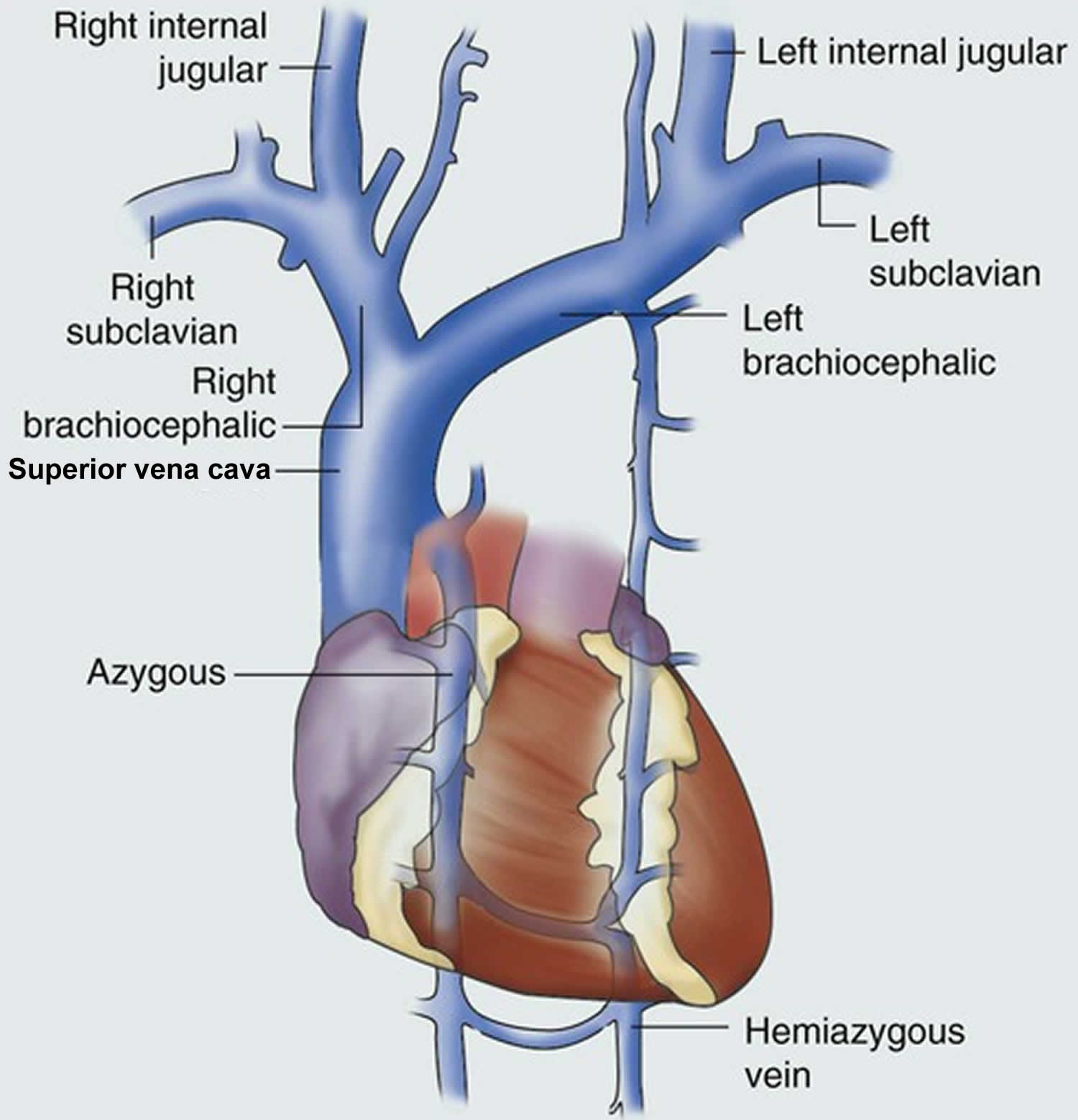
Hình 1. Giải phẫu tĩnh mạch chủ trên.
Các nhánh phụ lưu chủ yếu của SVC là tĩnh mạch azygos, chạy dọc theo bờ trước bên phải của đốt sống ngực đến mức ngã ba khí phế quản và thoát ra phía sau vào SVC. Các tĩnh mạch trung thất nhỏ khác cũng có thể chảy trực tiếp vào SVC và trở nên nổi bật hơn trên hình ảnh khi có tắc nghẽn SVC.
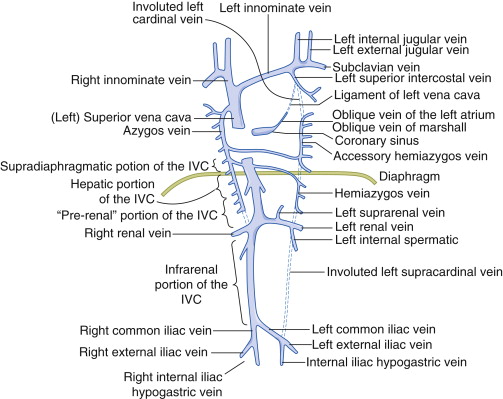
Hình 2. Giải phẫu tĩnh mạch chủ trên và các nhánh phụ lưu.
Việc làm quen với các biến thể giải phẫu của SVC là điều cần thiết đối với các nhà can thiệp, vì những biến thể này có thể ảnh hưởng đến hiệu suất tái thông mạch máu ở một số bệnh nhân. Tồn tại SVC bên trái là dị tật bẩm sinh phổ biến nhất, với tỷ lệ khoảng 0.3% đến 0.5% trong dân số nói chung và lên đến 5.2% ở bệnh nhân có tim bẩm sinh. SVC bên trái cùng tồn tại với SVC bên phải ở 80% đến 90% trường hợp. Khi có SVC đôi, SVC bên phải thoát vào tâm nhĩ phải như bình thường, trong khi SVC bên trái chảy vào xoang vành. SVC trái đơn độc, bao gồm SVC trái tồn tại với SVC phải vắng mặt, thoát vào tâm nhĩ phải qua xoang vành dãn.

Hình 3. Các biến thể giải phẫu của SVC.
(A) Type I: SVC ở bên phải bình thường.
(B) Type II: tồn tại SVC bên trái, vắng mặt SVC bên phải.
(C) Type IIIa: SVC hai bên kết nối với nhau.
(D) Type IIIb: SVC hai bên không kết nối với nhau.
(E) Có khả năng kết dính sợi xơ (các chấm đỏ) để khảo sát tại các điểm nối quan trọng trong SVC bên trái, xoang vành (CS), tâm nhĩ phải (RA) và tâm thất phải.
Mức độ phổ biến: Type II (40%), Type IIIa (10%), Type IIIb (50%).
3. Nguyên nhân gây hội chứng SVC
Trong lịch sử, trước khi có sự phát triển của thuốc kháng sinh, hội chứng SVC chủ yếu được cho là do phình động mạch chủ gây ra bởi giang mai (syphilitic aortic aneurysms) và bệnh hạch trung thất do lao (mediastinal adenopathy from tuberculosis). Hiện nay, các bệnh ác tính chiếm khoảng 70% các trường hợp và nguyên nhân lành tính liên quan đến thiết bị chiếm khoảng 30%. Một số ít hội chứng SVC lành tính không liên quan đến thiết bị, nguyên nhân chủ yếu là do xơ hóa trung thất. Bệnh nhân mắc hội chứng SVC lành tính thường trẻ hơn và có tuổi thọ cao hơn.
Tỷ lệ mắc hội chứng SVC liên quan đến thiết bị ngày càng tăng do việc sử dụng catheters, máy tạo nhịp, và máy khử rung tim ngày nay. Trong 1 nghiên cứu, 28% tất cả các hội chứng SVC có liên quan đến thiết bị. Huyết khối tĩnh mạch không triệu chứng (silent venous thrombosis) về mặt lâm sàng có thể xảy ra ở 30% bệnh nhân có dây dẫn tạo nhịp; tuy nhiên, tắc nghẽn SVC rất hiếm và chỉ gặp ở 0.1% đến 3.3% bệnh nhân. Hẹp ở ngã ba nhĩ-SVC xảy ra do sự lắng đọng fibrin trên bề mặt của các dây dẫn tạo nhịp và kết hợp vào các lỗ thông sau đó là viêm, xơ hóa thành mạch, hình thành huyết khối, và hẹp. Kích ứng cơ học mãn tính và phản ứng cơ thể với vật ngoại lai là những cơ chế thúc đẩy chính. Việc rút và tái đặt trở lại sau đó cũng gây ra chấn thương cơ học như là các yếu tố nguy cơ bổ sung cho tắc tĩnh mạch.
(1) Nguyên nhân ác tính (70%)
- Ung thư phổi không phải tế bào nhỏ (∼50%)
- Ung thư phổi tế bào nhỏ (∼25%)
- Lymphoma (∼10%)
- Các bệnh ung thư khác bao gồm u tuyến ức (thymoma), u tế bào mầm nguyên phát (primary germ cell neoplasms), u trung biểu mô (mesothelioma) và các khối u đặc có di căn hạch bạch huyết trung thất (ví dụ: ung thư vú) (∼15%)
(2) Nguyên nhân lành tính (∼30%)
- Ống thông tĩnh mạch trung tâm (central venous catheters), máy tạo nhịp tim (pacemakers), máy khử rung tim (defibrillator), ống thông chạy thận nhân tạo tại chỗ (indwelling hemodialysis catheters) (25–30%).
- Các nguyên nhân lành tính khác bao gồm xơ hóa do bức xạ (radiation fibrosis), nhiễm trùng (giang mai và lao – những nguyên nhân phổ biến nhất cách đây 50 năm), xơ hóa trung thất vô căn (idiopathic mediastinal fibrosis), tuyến giáp sau ức (retrosternal thyroid), phình động mạch chủ (aortic aneurysm), khối u lành tính, tụ máu trung thất, bệnh sarcoidosis, và các nguyên nhân do can thiệp y tế (∼1–5%).
4. Biểu hiện lâm sàng và phân độ lâm sàng
Biểu hiện lâm sàng khác nhau tùy thuộc vào mức độ, vị trí, và tốc độ bắt đầu tắc nghẽn, và sự hình thành các tĩnh mạch bàng hệ. Các triệu chứng biểu hiện phổ biến nhất bao gồm phù mặt và cổ, căng giãn các tĩnh mạch cổ và ngực, chảy nước mắt, và chóng mặt đặc biệt khi nghiêng người về phía trước. Bệnh nhân cũng có thể xuất hiện các triệu chứng thần kinh (nhức đầu, nhìn mờ, giảm ý thức), họng thanh quản (sưng lưỡi, khó thở), chi trên (phù) và mặt (phù kết mạc và phù quanh mắt). Bệnh nhân cũng thường có các triệu chứng tồi tệ hơn khi nằm ngửa. Hiếm khi có thể thấy giãn tĩnh mạch thực quản đoạn gần.
Tỷ lệ xuất hiện các dấu hiệu và triệu chứng:
- Phù mặt (60–100%)
- Các tĩnh mạch cổ căng phồng không đập (27–86%)
- Các tĩnh mạch ngực bị biến dạng (38–67%)
- Khó thở và ho (23–70%)
- Phù tay (14–75%)
- Khàn giọng hoặc thở rít (0–20%)
- Ngất hoặc nhức đầu (6–13%)
- Lẫn lộn, lơ mơ (0–5%)
Một số bệnh nhân có hội chứng SVC ác tính có thể xuất hiện với các triệu chứng đe dọa tính mạng của phù não, phù thanh quản và hầu họng do áp lực tĩnh mạch tăng đột ngột do SVC tắc nghẽn nhanh chóng. Sự tắc nghẽn SVC hiếm khi gây ra tổn thương huyết động trừ khi có sự chèn ép buồng tim do một bệnh lý ác tính tiềm ẩn. Tử vong cấp tính do hội chứng SVC là không phổ biến (0,3%); tuy nhiên, tuổi thọ trung bình của bệnh nhân mắc hội chứng SVC thứ phát sau bệnh ác tính chỉ là 6 tháng.
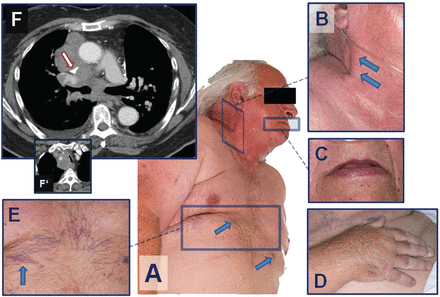
Hình 4. Các đặc điểm lâm sàng điển hình ở một bệnh nhân có hội chứng SVC do ung thư phổi tế bào nhỏ. Bệnh nhân này có biểu hiện khó thở và tăng PaCO2.
(A) Nhiều vùng sung huyết da mặt và cổ.
(B) Các tĩnh mạch cảnh méo mó.
(C) Môi tím tái.
(D) Cánh tay phải và bàn tay sưng to.
(E) Tuần hoàn bàng hệ đáng kể (mũi tên).
(F) CT cho thấy chèn ép SVC (mũi tên) do khối trung thất lớn.
(F’) Gây chèn ép và đẩy lệch khí quản, và gây thở rít.
Yu và cộng sự đã mô tả mức độ của hội chứng SVC dựa trên biểu hiện lâm sàng. Hệ thống tính điểm do các tác giả này đề xuất, với phạm vi từ grade 0 đến grade 5, có thể hữu ích trong việc tiếp cận chẩn đoán và xác định phương pháp điều trị. Hệ thống Kishi score là một hệ thống đánh giá khác được phát triển để hỗ trợ việc đưa ra quyết định liên quan đến liệu pháp đặt stent. Nó bao gồm các dấu hiệu và triệu chứng về thần kinh, thanh quản, mặt, và tim mạch. Theo thang điểm này, Kishi score từ 4 điểm trở lên cảnh báo cần can thiệp nội mạch.
Phân loại Hội chứng SVC theo Yu et al:
- Grade 0: Không có triệu chứng (SVC trên hình ảnh không triệu chứng)
- Grade 1: Nhẹ (phù đầu hoặc cổ)
- Grade 2: Trung bình (phù ở đầu hoặc cổ với suy giảm chức năng)
- Grade 3: Nặng (phù não/phù thanh quản nhẹ đến trung bình, hoặc giảm chức năng tim).
- Grade 4: Đe dọa tính mạng (phù não đáng kể, phù thanh quản, huyết động bị ảnh hưởng)
- Grade 5: Tử vong
5. Các dạng tắc nghẽn và các hệ thống bàng hệ
Trong tắc nghẽn SVC, dòng máu được chuyển hướng đến tâm nhĩ phải thông qua một mạng lưới tĩnh mạch bàng hệ, có thể mất vài tuần để đáp ứng lưu lượng máu thông thường của SVC. Mức độ nghiêm trọng của hội chứng SVC tỷ lệ nghịch với sự phát triển của các tĩnh mạch bàng hệ này và tốc độ phát triển của tắc nghẽn SVC. Tắc nghẽn SVC thường làm cho áp lực tĩnh mạch tăng cao từ 20 đến 40 mmHg gần chỗ tắc nghẽn. Áp lực tĩnh mạch tăng lên này tạo ra các triệu chứng phù mặt, cổ và thành ngực. Có 4 con đường phụ chủ yếu: 1) hệ thống tĩnh mạch azygous, là hệ thống tĩnh mạch lớn nhất và bao gồm các azygos (tĩnh mạch đơn), hemiazygos (tĩnh mạch bán đơn), các tĩnh mạch liên sườn và thắt lưng; 2) con đường ngực trong; 3) con đường dẫn lưu ngực ngoài; 4) con đường tĩnh mạch đốt sống.

Hình 5. Bốn hệ thống bàng hệ chính trong tắc nghẽn SVC.
(1)Hệ thống azygos (màu hồng) bao gồm các tĩnh mạch azygos, tĩnh mạch hemiazygos, các tĩnh mạch liên sườn và thắt lưng. Cần lưu ý, sự tắc nghẽn SVC phía trên azygous sử dụng con đường này, dẫn đến các triệu chứng nhẹ hơn.
(2)Hệ thống ngực trong (màu xanh) bao gồm các tĩnh mạch ngực trong, thượng vị trên và dưới, và tĩnh mạch ngực nông (không dán nhãn).
(3)Hệ thống ngực ngoài (không dán nhãn) bao gồm các tĩnh mạch nhỏ chủ yếu bao gồm các tĩnh mạch ngực ngoài, tĩnh mạch ngực-thượng vị, tĩnh mạch mũ nông, và tĩnh mạch đùi.
(4)Hệ thống đốt sống (màu tím) kết hợp với tĩnh mạch azygos và các tĩnh mạch ngực trong thông qua các tĩnh mạch đốt sống, liên sườn và thắt lưng.
Phân loại giải phẫu của tắc nghẽn SVC bao gồm 3 mức độ tắc nghẽn: tắc nghẽn SVC phía trên gần với tĩnh mạch azygos, tắc nghẽn ở ngang mức tĩnh mạch azygos và tắc nghẽn ở xa tĩnh mạch azygos. Tắc nghẽn phía trên tĩnh mạch azygos làm cho máu trở về tâm nhĩ phải thông qua hệ thống ayzgos và các tĩnh mạch liên sườn để vào SVC. Trong tắc nghẽn SVC ở ngang mức azygos, máu không thể vào SVC thông qua hệ thống azygos và buộc phải đi qua các tĩnh mạch bàng hệ khác, dẫn vào IVC và sau đó vào tâm nhĩ phải. Tắc nghẽn SVC dưới tĩnh mạch azygos, máu sẽ được chuyển hướng qua hệ thống azygos và hemi-azygos ngược dòng cuối cùng đến IVC, do đó gây ra các triệu chứng ít nghiêm trọng hơn. Tuy nhiên, trong nhiều trường hợp, các tĩnh mạch cánh tay đầu (hoặc các phần của chúng) cũng có liên quan, do đó các tĩnh mạch bàng hệ được hình thành nhiều và có thể bao gồm bất kỳ con đường nào đã được liệt kê trước đó.
 Hình 6. Phân loại giải phẫu của tắc nghẽn SVC
Hình 6. Phân loại giải phẫu của tắc nghẽn SVC
(A) Sự tắc nghẽn của SVC liên quan đến các tĩnh mạch cánh tay đầu trái và phải: các tĩnh mạch bàng hệ được hình thành có thể có nhiều và có thể bao gồm bất kỳ con đường nào được mô tả.
(B) Sự tắc nghẽn của SVC gần điểm vào tĩnh mạch azygos (phía trên tĩnh mạch azygos): dòng máu được dẫn đến tĩnh mạch azygos qua tĩnh mạch liên sườn trên bên phải.
(C) Sự tắc nghẽn của SVC ở mức azygos: hệ thống tĩnh mạch azygos không thể sử dụng như một con đường bàng hệ; các tĩnh mạch bàng hệ ở thành ngực khác như tĩnh mạch thượng vị trên và tĩnh mạch ngực trong được hình thành, và các triệu chứng thường nghiêm trọng hơn.
(D) Sự tắc nghẽn của SVC xa đến điểm vào azygos (phía dưới tĩnh mạch azygos): dòng máu ngược dòng sử dụng các tĩnh mạch azygos và hemiazygos đến IVC dẫn đến các triệu chứng nhẹ hơn.
Không có tiêu chuẩn để phân loại các thể tắc nghẽn SVC. Phương pháp được sử dụng rộng rãi nhất là phương pháp Stanford, phân loại tắc nghẽn SVC bằng chụp hệ tĩnh mạch (venography): Type I là tắc nghẽn SVC phía trên tĩnh mạch azygous với SVC dưới tĩnh mạch azygous còn lưu thông và có dòng chảy ngược từ tĩnh mạch azygos. Type II là loại tắc nghẽn gần hoàn toàn (> 90%) của SVC phía trên tĩnh mạch azygos với tĩnh mạch azygos còn lưu thông có dòng chảy ngược dòng. Type III là tắc nghẽn hoàn toàn SVC với tồn tại dòng chảy ngược trong tĩnh mạch azygos. Cuối cùng, type IV là sự tặc nghẽn hoàn toàn của SVC và 1 hoặc nhiều nhánh phụ lưu chính của tĩnh mạch chủ bao gồm hệ thống azygos. Phương pháp Stanford được phát triển để giúp xác định những bệnh nhân có nguy cơ tổn thương đường thở hoặc não cần can thiệp phẫu thuật, do đó nó không được áp dụng rộng rãi ở những bệnh nhân có triệu chứng ít nghiêm trọng hơn.

Hình 7. Phân loại Stanford các giai đoạn tắc SVC trên hình ảnh học. Hệ thống này được phát triển để hỗ trợ xác định những bệnh nhân có nguy cơ tổn thương đường thở hoặc não đáng kể và do đó đảm bảo can thiệp nhanh chóng.
(A) Stanford type I: tắc nghẽn SVC nhẹ, với tỷ lệ dưới 90%.
(B) Stanford type II: hẹp SVC grade cao (mức độ hẹp 90-100%).
(C): Stanford type III: tắc nghẽn hoàn toàn SVC và dòng chảy nổi bật qua các tĩnh mạch bàng hệ, nhưng không có sự tham gia của các tĩnh mạch ngực trong và thượng vị.
(D): Stanford type IV: tắc nghẽn hoàn toàn SVC và dòng chảy nổi bật qua các tĩnh mạch bàng hệ, các tĩnh mạch ngực trong và thượng vị.
Không có phương pháp phân loại hiện có nào bao gồm cả vị trí giải phẫu và mức độ nghiêm trọng của tắc nghẽn. Để giải quyết vấn đề này, các tác giả đã đề xuất một hệ thống phân loại dựa trên cả vị trí và mức độ nghiêm trọng. Khi được sử dụng cùng với các triệu chứng lâm sàng, hệ thống này có thể hữu ích để hướng dẫn quản lý tổng thể và tạo điều kiện giao tiếp giữa các bác sĩ lâm sàng. Phân loại đề xuất có thể được sử dụng rộng rãi bởi các nhà nghiên cứu, bác sĩ lâm sàng, và bác sĩ can thiệp khác với hy vọng xác nhận mối liên quan với các kết quả thủ tục và dài hạn khác nhau.

Hình 8. Phân loại đề xuất của tắc SVC dựa trên vị trí và mức độ nghiêm trọng. Hệ thống phân loại được đề xuất xem xét vị trí giải phẫu và mức độ nghiêm trọng của tắc nghẽn SVC. Khi được sử dụng cùng với các triệu chứng lâm sàng, nó có thể được sử dụng để hướng dẫn xử trí và tạo điều kiện giao tiếp giữa các bác sĩ lâm sàng.
6. Tiếp cận chẩn đoán
Chẩn đoán hội chứng SVC dựa trên biểu hiện lâm sàng và nghiên cứu hình ảnh. Các phương thức chẩn đoán hình ảnh bao gồm X quang ngực, CT có thuốc cản quang, siêu âm, chụp tĩnh mạch số hóa xóa nền dựa vào catheter, và MRI. Chụp CT có thuốc cản quang cung cấp hình ảnh tối ưu về SVC và có thể xác định mức độ tắc nghẽn tĩnh mạch, phân biệt huyết khối với chèn ép từ bên ngoài và xác định tuần hoàn bàng hệ. Các phát hiện trên CT bao gồm sự khuyết thuốc cản quang, sự hiện diện của khiếm khuyết lấp đầy lòng mạch hoặc hẹp SVC, và quan sát hệ thống bàng hệ. Sự hiện diện của các mạch máu bàng hệ trên CT là một yếu tố dự đoán rất chính xác về hội chứng SVC có triệu chứng và liên quan đến lâm sàng, trong khi việc xác định riêng rẽ về tắc nghẽn SVC là một yếu tố dự đoán ít đặc hiệu hơn. Lưu ý rằng hệ thống tĩnh mạch bàng hệ vẫn tồn tại trên hình ảnh sau khi can thiệp nội mạch, ngay cả khi các triệu chứng lâm sàng được cải thiện.
Siêu âm hai tay rất hữu ích để đánh giá huyết khối trong tĩnh mạch cảnh, tĩnh mạch dưới đòn, và tĩnh mạch nách. Nó cũng hữu ích trong việc xác định huyết khối liên quan đến các thiết bị nằm bên trong và xác định vị trí ở chi trên để tiếp cận chụp tĩnh mạch và can thiệp nội mạch. Tuy nhiên, việc quan sát trực tiếp SVC và các tĩnh mạch cánh tay đầu là một thách thức, do các xương sườn và phổi che khuất. Chụp tĩnh mạch số hóa xóa nền là tiêu chuẩn vàng để đánh giá tắc nghẽn SVC, bao gồm cả sự hiện diện của huyết khối. Chụp tĩnh mạch xác định các đường dẫn tĩnh mạch dẫn lưu bàng hệ và xác định mức độ nghiêm trọng của tắc nghẽn, đồng thời cho phép bác sĩ can thiệp phát triển một chiến lược tái thông mạch dứt điểm.
Tiếp cận đường tĩnh mạch cho phép đánh giá ý nghĩa huyết động của tắc nghẽn, cũng như sự hiện diện của bất kỳ dị tật bẩm sinh nào. Hạn chế của phương pháp chụp tĩnh mạch xâm lấn là không có khả năng đánh giá nguyên nhân chèn ép SVC từ bên ngoài, ngay cả khi kết hợp với siêu âm nội mạch. Chụp MRV (magnetic resonance venography) từ là một phương pháp thay thế ở những bệnh nhân bị dị ứng thuốc cản quang, hoặc trong những trường hợp không thể tiếp cận được bằng đường nội tĩnh mạch. Chụp MRV có độ nhạy và độ đặc hiệu tương đương, khi so sánh với phương pháp chụp tĩnh mạch thông thường trong việc xác định tắc nghẽn SVC.
7. Tiếp cận điều trị
7.1. Tổng quan
Phương pháp điều trị ở bệnh nhân mắc hội chứng SVC nên là đa mô thức và có thể bao gồm các chuyên khoa như ung bướu, hô hấp, CĐHA, ngoại khoa, chuyên khoa mạch máu và can thiệp nội mạch. Các lựa chọn điều trị có thể bao gồm hóa trị có hoặc không kèm xạ trị, phẫu thuật bắc cầu, hoặc can thiệp nội mạch như nong mạch, đặt stent, và loại bỏ huyết khối bằng catheter.
Xử trí ban đầu cho tất cả bệnh nhân có hội chứng SVC bao gồm kê cao đầu để giảm áp lực thủy tĩnh ở đầu và cổ. Việc quản lý hội chứng SVC liên quan đến bệnh ác tính tập trung vào việc điều trị giảm nhẹ các triệu chứng ngay lập tức, cũng như điều trị bệnh ác tính. Trong các tình huống nguy hiểm đến tính mạng, việc thiết lập ban đầu với các ABC (đường thở, hô hấp, tuần hoàn) nhanh chóng sau đó là tái thông nội mạch có hoặc không đặt stent để nhanh chóng giải quyết tắc nghẽn và làm giảm các triệu chứng.
Glucocorticoid đường tiêm và thuốc lợi tiểu quai là những thuốc thường được sử dụng trong hội chứng SVC, nhưng thiếu dữ liệu về tính hiệu quả của chúng. Steroid thường được sử dụng để dự phòng ngăn ngừa phù nề do bức xạ và cũng được sử dụng ở những bệnh nhân bị tổn thương đường thở. Nếu sử dụng steroid, chúng phải có hiệu lực cao và thời gian nên được giới hạn.
Quản lý được hướng dẫn bởi mức độ nghiêm trọng của các triệu chứng và xác định bệnh ác tính cơ bản. Chẩn đoán mô học là rất quan trọng để đưa ra một kế hoạch điều trị cụ thể theo từng giai đoạn và từng khối u. Tùy thuộc vào căn nguyên cơ bản, một số bệnh nhân có thể đạt được khả năng sống sót và chữa khỏi lâu dài mà không tái phát.

Hình 9. Sơ đồ quản lý được đề xuất của hội chứng SVC dựa trên mức độ nghiêm trọng của các triệu chứng và các nguyên nhân phổ biến.
7.2. Xạ trị
Theo truyền thống, hội chứng SVC được xem như một tình trạng bệnh khẩn cấp tương đối và xạ trị được coi là phương pháp điều trị đầu tiên. Bắt đầu thực hiện xạ trị khẩn cấp được cho là cách nhanh nhất để giảm tắc nghẽn ở những bệnh nhân có các triệu chứng đe dọa tính mạng. Gần đây, xạ trị ít được sử dụng hơn vì những lý do sau: chẩn đoán mô học sau xạ trị là không thể trong khoảng 40% trường hợp. Xạ trị dẫn đến giảm triệu chứng ở khoảng 80% bệnh nhân; tuy nhiên, có thể mất từ 3 ngày đến 4 tuần để cải thiện. Hơn nữa, có đến 20% bệnh nhân không giảm được triệu chứng. Xạ trị làm giảm gánh nặng khối u, nhưng lợi ích thường là tạm thời với 5% đến 30% bệnh nhân bị hội chứng SVC tái phát. Ngược lại, đặt stent nội mạch giúp giảm nhanh các triệu chứng hơn.
7.3. Can thiệp phẫu thuật
Can thiệp phẫu thuật mở, chẳng hạn như phẫu thuật bắc cầu và tái tạo SVC, được dành riêng cho các trường hợp huyết khối hoặc tắc tĩnh mạch diện rộng có nhiều triệu chứng và không thể can thiệp nội mạch. Phẫu thuật mở bắc cầu từng được coi là phương pháp điều trị chính cho hội chứng SVC ở những bệnh nhân có căn nguyên lành tính, đặc biệt là ở những người có tuổi thọ cao. Phẫu thuật bắc cầu thường được thực hiện từ tĩnh mạch vô danh hoặc tĩnh mạch cảnh đến tiểu nhĩ phải hoặc SVC bằng cách sử dụng mảnh ghép tĩnh mạch hiển. Gần một nửa số ca phẫu thuật bắc cầu cuối cùng cần can thiệp nội mạch để duy trì tuần hoàn thứ cấp.
7.4. Liệu pháp nội mạch
Trong hơn 2 thập kỷ qua, can thiệp nội mạch bằng đặt stent đã trở thành tiêu chuẩn điều trị tắc nghẽn SVC, cho cả căn nguyên lành tính và ác tính. Các lợi ích của liệu pháp nội mạch bao gồm giải quyết nhanh các triệu chứng với tỷ lệ thành công của kỹ thuật cao và ít biến chứng. Ngoài ra, liệu pháp nội mạch không ảnh hưởng xấu đến kết quả của phẫu thuật mổ hở, nếu bệnh nhân cần phẫu thuật sau đó. Liệu pháp nội mạch không ảnh hưởng đến chẩn đoán mô học tiếp theo và có thể được kết hợp với các phương thức điều trị khác bao gồm hóa trị và xạ trị nếu cần.
Hiện tại, liệu pháp nội mạch được sử dụng như là phương pháp đầu tay cho phần lớn bệnh nhân mắc hội chứng SVC, đặc biệt là những bệnh nhân có các triệu chứng đe dọa tính mạng như phù não hoặc phù thanh quản hoặc ngất do tư thế. Mặc dù không có các nghiên cứu tiến cứu ngẫu nhiên về liệu pháp nội mạch trong việc điều trị hội chứng SVC, dữ liệu quan sát cho thấy tỷ lệ thành công kỹ thuật cao là 80% đến 98%, với việc giảm triệu chứng ở >90% bệnh nhân. Kết quả cũng có vẻ lâu bền với tỷ lệ tái thông từ 4.3% đến 29.5% (trung bình 11.9%) và tỷ lệ tái phát 1.2% đến 20.5% (trung bình 10.5%).
Điều trị tối ưu hội chứng SVC liên quan đến máy tạo nhịp tim hoặc máy khử rung tim vẫn chưa được xác định rõ, vì có rất ít bằng chứng hướng dẫn bác sĩ lâm sàng. Sự hiện diện của các chuyển đạo làm hạn chế các phương pháp điều trị có thể có, đặc biệt là việc triển khai đặt stent. Chỉ riêng phương pháp nong mạch bằng bóng đã được sử dụng để giải quyết tình trạng hẹp tĩnh mạch do dây dẫn tạo nhịp; trong 1 nghiên cứu, tỷ lệ khỏi bệnh sau can thiệp được ghi nhận là 86% sau 12 tháng. Trong trường hợp có thể cần đặt stent để duy trì dòng chảy, các dây dẫn phải được loại bỏ trước khi đặt stent để tránh bị mắc kẹt. Tỷ lệ mắc hội chứng SVC sau khi đặt máy tạo nhịp tim hoặc cấy dây dẫn máy khử rung tim là một tác dụng ngoại ý rất hiếm gặp và kháng đông thường quy như một biện pháp phòng ngừa không được khuyến cáo ngay cả ở những bệnh nhân có nguy cơ cao, vì nguy cơ chảy máu nhiều hơn lợi ích.
7.5. Hội chứng SVC với huyết khối
Trong một số trường hợp tắc nghẽn SVC, có thể có sự hiện diện của huyết khối bao trùm, có thể liên quan đến sự ngưng trệ của dòng chảy, tình trạng tăng đông do bệnh lý ác tính tiềm ẩn hoặc sự hiện diện của các ống thông trong lòng mạch. Ở những bệnh nhân như vậy, biểu hiện thường cấp tính và trong quá trình can thiệp dây dẫn (guidewire) thường dễ dàng đi qua đoạn bị tắc. Loại bỏ huyết khối bằng catheter hoặc chọc hút huyết khối (aspiration thrombectomy) được khuyến cáo trước khi tái thông mạch máu, để ngăn ngừa thuyên tắc phổi và giảm tổn thương do điều trị.
Nên tiến hành tiêu huyết khối (thrombolysis) hoặc lấy bỏ huyết khối (thrombectomy) trong vòng 2 đến 5 ngày kể từ khi có triệu chứng để điều trị có hiệu quả. Nếu sau vài ngày, khả năng ly giải cục máu đông (clot lysis) thành công sẽ giảm đáng kể vì cục máu đông trở nên có tổ chức. Lấy huyết khối bằng catheter đã được chứng minh là an toàn và hiệu quả ở những bệnh nhân bị ung thư và không ung thư. Nếu bệnh nhân có nguy cơ chảy máu cao và chống chỉ định tuyệt đối với thuốc tan huyết khối thì kỹ thuật lấy huyết khối cơ học có thể được ưu tiên hơn.

Hình 10. Tắc nghẽn SVC do huyết khối liên quan đến catheter.
(A) Bệnh nhân 29 tuổi bị tắc nghẽn tim bẩm sinh sau khi đặt máy tạo nhịp vĩnh viễn với biểu hiện tắc SVC; CT coronal cho thấy tĩnh mạch azygos nổi rõ (mũi tên đỏ) với các tĩnh mạch bàng hệ bên phải.
(B) CT sagittal của tĩnh mạch azogyos dãn với các tĩnh mạch bàng hệ (các mũi tên màu đỏ).
(C) Hình ảnh tái tạo ba chiều cho thấy tĩnh mạch azogyos và các tĩnh mạch bàng hệ.
8. Các kỹ thuật nội mạch
8.1. Tổng quan
Hầu hết các thủ thuật này được thực hiện ở tư thế nằm ngửa trong phòng can thiệp nội mạch với gây tê vùng và an thần có ý thức. Một số bệnh nhân có thể cần kê cao đầu hoặc cần gây mê toàn thân với thở máy tùy thuộc vào việc các triệu chứng xấu đi khi nằm thẳng hoặc sự hiện diện của phù đường thở. Trong quá trình nong mạch / đặt stent, có thể cần dùng thêm thuốc opiate, vì sự dãn chỗ hẹp có thể gây khó chịu.
Tiếp cận bằng tĩnh mạch có thể thực hiện dưới hướng dẫn của siêu âm. Vị trí và mức độ tắc nghẽn sẽ hướng dẫn việc lựa chọn vị trí tiếp cận. Ở những bệnh nhân có tổn thương không tắc nghẽn, một vị trí tiếp cận duy nhất thường là đủ, mặc dù tiếp cận kép có thể cung cấp nhiều lựa chọn hơn cho hình ảnh và hỗ trợ tốt hơn cho việc cung cấp thiết bị. Nhiều nhà can thiệp thích phương pháp tiếp cận ở vùng đùi để thuận tiện. Ở những bệnh nhân bị tắc SVC toàn bộ, nên tiếp cận bổ sung để quá trình tái thông mạch thành công.
Hình ảnh trực tiếp từ trước cho phép đánh giá tốt hơn chiều dài tổn thương và tạo điều kiện thuận lợi cho việc băng qua tổn thương với dây dẫn. Các tùy chọn để tiếp cận từ hướng phía trên tới SVC bao gồm các tĩnh mạch nền cánh tay, tĩnh mạch cánh tay, tĩnh mạch nách, hoặc tĩnh mạch cảnh trong. Ở những bệnh nhân bị hẹp hoặc tắc SVC mở rộng vào tĩnh mạch cánh tay đầu hoặc tĩnh mạch dưới đòn, việc tiếp cận từ tĩnh mạch cánh tay hoặc tĩnh mạch nền cánh tay một bên sẽ tạo điều kiện đi qua tổn thương thành công. Chụp tĩnh mạch được cải tiến với kỹ thuật số hóa xóa nền cùng với tính năng giữ theo nhịp thở sẽ cung cấp hình ảnh tối ưu. Ở những bệnh nhân bị tắc toàn bộ, có thể cần dùng thuốc cản quang ở cả hai cánh tay để xác định hướng dòng chảy, tĩnh mạch bàng hệ, và sự hiện diện của huyết khối.

Hình 11. Trường hợp minh họa đặt stent SVC ở một phụ nữ 55 tuổi bị ung thư phổi tế bào nhỏ và tắc nghẽn SVC Stanford type II khi nhập viện.
(A) Lòng mạch thu hẹp >90% (mũi tên đỏ). Lưu ý sự giãn nở sung huyết của các tĩnh mạch dẫn lưu vào SVC (các mũi tên màu xanh).
(B) Sau khi đặt một stent Sinus XXL 22 x 60 mm trong SVC, tình trạng lưu thông của SVC đã được khôi phục hoàn toàn. Các tĩnh mạch sung huyết dẫn lưu vào SVC cũng biến mất ngay sau khi đặt stent.
8.2. Tái điều chỉnh tắc nghẽn SVC toàn bộ mãn tính
Khi đã xác định được các góc hình ảnh tối ưu và độ dài của đoạn tắc, thì một dây dẫn sẽ được sử dụng để xuyên qua tổn thương. Việc sử dụng đúng đắn nhiều vị trí truy cập cho phép nhà nhà can thiệp điều khiển dây dẫn với độ chính xác cao hơn. Nhiều dây dẫn và kỹ thuật khác nhau có thể được sử dụng.
Trước tiên, nhiều nhà can thiệp sẽ cố gắng vượt qua với một dây dẫn ái nước (ví dụ, dây trượt, có góc cạnh hoặc thẳng, cứng hoặc mềm), được hỗ trợ bởi catheter chẩn đoán. Nếu không thể vượt qua tổn thương một cách dễ dàng, có thể sử dụng các dây dẫn đường và thiết bị xuyên qua tích cực hơn (ví dụ trong kiểu kiểu tắc nghẽn toàn bộ). Các thiết bị cơ học (ví dụ: Frontrunner [Cordis, Miami Lakes, Florida]), năng lượng sóng RF, chiếu xạ laser, hoặc tái thông bén hơn với dây dẫn ái nước đôi khi có thể được sử dụng để bắt đầu; tuy nhiên, những loại này phải được sử dụng hết sức thận trọng, vì biến chứng nguy kịch gây vỡ hoặc thủng SVC.
Sau khi xuyên qua tổn thương thành công, khuyến cáo nên nong trước bằng bóng có kích thước nhỏ (2 đến 4 mm) ở chỗ hẹp. Tiếp theo là nong tuần tự với đường kính bóng tăng dần, đánh giá phản ứng của mạch và phản ứng lâm sàng của bệnh nhân (chẳng hạn như biểu hiện đau nhiều) với mỗi lần nong. Nong trước tạo điều kiện thuận lợi cho việc đặt stent, nhưng kích thước bóng quá lớn >16mm có liên quan đến tăng nguy cơ vỡ SVC, rối loạn nhịp tim, chèn ép màng ngoài tim, hoặc ngừng tim.
8.3. Lựa chọn và đặt stent
Phương pháp nong mạch bằng bóng đơn thuần không cần điều trị hỗ trợ và có thể làm dòng chảy được phục hồi nhanh và giảm các triệu chứng; tuy nhiên, hiện tượng tái hẹp sớm đáng kể là phổ biến, do sự chèn ép bên ngoài và bản chất xơ hóa của mô quanh mạch. Theo đó, hiện nay tái thông SVC bao gồm đặt stent trong đa số các trường hợp. Việc lựa chọn stent phụ thuộc vào nhiều yếu tố bao gồm mức độ nghiêm trọng, độ dài và độ ngoằn ngoèo của SVC và khả năng chống giãn mạch.
Dữ liệu trước phẫu thuật từ hình ảnh CT có thể hữu ích để chọn stent có kích thước và chiều dài phù hợp. Các lựa chọn stent bao gồm loại stent có thể nong bằng bóng với loại stent tự giãn, stent có bao phủ với loại không bao phủ. Các loại stent được sử dụng phổ biến nhất là stent có bóng (ví dụ, Palmaz stent [Cordis]), Wallstent tự dãn (Boston Scientific, Natick, Massachusetts) và Z-stent Gianturco (Cook Medical, Bloomington, Indiana).
Các stent có thể nong bằng bóng cho phép đặt chính xác với tỷ lệ di chuyển giảm xuống ngoài lực hướng tâm cao hơn để khắc phục nguy cơ tái hẹp. Các stent tự giãn phù hợp hơn với thành tĩnh mạch và có khả năng chống bị ép hai đầu. Điều này cho phép thay đổi thể tích của lồng ngực bệnh nhân và đường kính mạch máu gây ra bởi hô hấp. Để đảm bảo độ che phủ của tổn thương, thường phải sử dụng các stent tự giãn dài hơn, điều này có thể dẫn đến cầm tù các tĩnh mạch cánh tay đầu hai bên.
Nhiều nhà can thiệp hiện đang thích sử dụng các loại stent được che phủ, chẳng hạn như Gore Viabahn (Gore, Newark, Delaware) và iCast (Atrium, Dallas, Texas), dựa trên các báo cáo về thời gian sử dụng 12 tháng tốt hơn so với các loại stent không được che phủ. Các stent được che phủ có thể ngăn ngừa sự thoát mạch nguy hiểm trong trường hợp SVC bị gián đoạn hoặc vỡ; tuy nhiên, cần thận trọng để tránh loại trừ các tĩnh mạch bàng hệ khi sử dụng các loại stent được che phủ. Cho đến nay, sự khác biệt về tỷ lệ thành công trên lâm sàng và tỷ lệ tử vong tổng thể của bệnh nhân vẫn chưa được chứng minh giữa các loại stent khác nhau.
Cục quản lý thực phẩm và dược phẩm (The Food and Drug Administration) gần đây đã phê duyệt các stent tĩnh mạch chuyên dụng (Venovo [Bard, Minneapolis, Minnesota] và Vici [Boston Scientific]). VIRTUS và VERNACULAR cho thấy tỷ lệ khả dụng tuyệt vời của các stent tĩnh mạch chuyên dụng này trong tắc nghẽn tĩnh mạch chậu đùi. Dữ liệu về việc sử dụng các stent mới này trong hội chứng SVC vẫn chưa có sẵn. Cuối cùng, việc sử dụng một stent-graft lai với phần trung tâm được che phủ và các đầu không được che phủ, được thiết kế để đặt shunt hệ thống cửa chủ thông qua tĩnh mạch cảnh và tĩnh mạch gan (Viatorr stent-graft [Gore, Flagstaff, Arizona]) đã được sử dụng thành công cho hội chứng SVC.
8.4. Mở rộng tắc nghẽn SVC thành các tĩnh mạch cánh tay
Khi tình trạng tắc nghẽn SVC xảy ra có sự liên quan của tĩnh mạch cánh tay đầu hai, việc giải quyết tắc nghẽn ở một trong các tĩnh mạch cánh tay đầu bị tắc thường là đủ để giải quyết triệu chứng. Dinkel và cộng sự đã chỉ ra rằng việc tái thông và đặt stent của 1 thay vì cả 2 tĩnh mạch cánh tay đầu có liên quan đến tỷ lệ biến chứng và huyết khối trong stent thấp hơn. Hầu hết các nhà can thiệp đều tránh đặt hai stent đối diện chạm nhau nếu đường kính SVC <15 mm.
Trong một số trường hợp nhất định, chẳng hạn như khi tắc liên quan đến chỗ hợp lưu của các tĩnh mạch cánh tay đầu, việc tái tạo chỗ phân nhánh SVC có thể thích hợp. Thông thường, việc tái tạo này được thực hiện bằng cách sử dụng stents kép (kissing stents), còn được gọi là nòng đôi (double barrel), bằng cách kéo dài stent từ SVC vào các tĩnh mạch cánh tay đầu phải và trái.
Tùy thuộc vào giải phẫu ở mỗi bệnh nhân, phương pháp tiếp cận ống quần (pant legs approach) có thể được đảm bảo, trong đó một stent riêng biệt được triển khai trong SVC, trước khi đặt 2 kissing stent vào mỗi nhánh của mỗi tĩnh mạch cánh tay đầu. Lợi ích của việc có một giá đỡ SVC mà trong đó các stent tĩnh mạch cánh tay có thể được tái tạo ổn định và bền hơn, mặc dù vẫn chưa có dữ liệu để hỗ trợ điều này.
Trong quá trình tái tạo lại phân nhánh SVC, nếu stent tự giãn được sử dụng như các chi kéo dài từ SVC vào các tĩnh mạch cánh tay đầu, việc triển khai các stent có thể giãn bằng bóng bên trong các thiết bị tự giãn nở có thể được thực hiện để tăng cường độ chắc chắn, cung cấp thêm độ bao phủ , và đảm bảo diện tích lòng mạch tối đa.
Cho đến nay, điều này được thực hiện phổ biến nhất với stent Palmaz trong Wallstents, nhưng stent dày gấp đôi cũng có thể được thực hiện với các thiết bị mới hơn. Từ góc độ lâm sàng, việc tái tạo lại phân nhánh SVC với phương pháp tiếp cận hai nòng tạo ra các ống dẫn tự nhiên hai bên để hỗ trợ phần cứng trong tương lai, bao gồm ống thông và máy tạo nhịp hoặc dây dẫn máy khử rung.
Ít được sử dụng hơn là phương pháp tiếp cận chữ Y (Y approach), trong đó một stent được đưa qua thành của một stent khác, sau đó được đặt để tạo thành hình chữ Y. Ngược lại với phương pháp stent song song, phương pháp chữ Y có ít cơ hội di chuyển stent hơn và tạo ra một lòng mạch duy nhất lớn hơn trong SVC, điều này có thể làm giảm tỷ lệ tắc nghẽn sau đó. Tuy nhiên, có khả năng trượt một stent này qua thành của stent khác, điều này có thể làm suy yếu tính toàn vẹn của stent, dẫn đến gãy và trật stent.
8.5. Liệu pháp chống đông sau khi tái thông nội mạch
Dữ liệu hướng dẫn ra quyết định liên quan đến liệu pháp dược lý sau tái thông mạch chưa đầy đủ và thực hành lâm sàng cũng khác nhau tùy nơi. Nói chung, thuốc kháng đông nên được giữ lại. Việc tiêm bolus tĩnh mạch ban đầu với heparin liều thấp có thể cần thận trọng cho đến khi có đạt được sự tiếp cận an toàn ở tất cả các vị trí tĩnh mạch, tổn thương được xuyên qua và xác định được vị trí trong lòng mạch. Tại thời điểm đó, sử dụng heparin liều đầy đủ để đạt được thời gian đông máu hoạt hóa. Một thời gian ngắn điều trị với 3 liệu pháp (chống đông máu, aspirin liều thấp, và kháng kết tập tiểu cầu) có thể được xem xét ở những bệnh nhân bị tắc mạch huyết khối nếu không có nguy cơ chảy máu quá cao. Ở những bệnh nhân bị tắc nghẽn không do huyết khối, liệu pháp kháng kết tập tiểu cầu kép với aspirin và thienopyridine thường được sử dụng trong một tháng hoặc lâu hơn, mặc dù cho đến nay vẫn chưa có bằng chứng chứng minh điều này.
8.6. Biến chứng của liệu pháp nội mạch
Các biến chứng liên quan đến việc tái thông mạch SVC là thấp có thể chấp nhận được và được giảm thiểu bằng kinh nghiệm và sự thận trọng của nhà can thiệp. Các biến chứng nhỏ rất ít xảy ra, bao gồm tụ máu và nhiễm trùng cục bộ tại chỗ chọc (3.2%). Các biến chứng lớn bao gồm chèn ép màng ngoài tim, vỡ SVC, lệch stent, tái hẹp trong stent, phù phổi, chảy máu nhiều, thuyên tắc phổi ,và tổn thương tim; những điều này có thể rất nghiêm trọng, thậm chí gây tử vong. Tỷ lệ tích lũy của các biến chứng này là <8%. Ở những bệnh nhân có hội chứng SVC ác tính, đặt stent có tỷ lệ tử vong do thủ thuật là 2%.
Chèn ép màng ngoài tim là một biến chứng hiếm gặp (0.1% đến 1.8%) nhưng gây ra hậu quả đáng sợ và có khả năng gây tử vong cao, đặc biệt khi kích thước bóng <16 mm được sử dụng. Những bệnh nhân đã trải qua xạ trị gần đây có thể tăng nguy cơ vỡ SVC và cần hết sức thận trọng đối với những bệnh nhân này. Các cơ sở cung cấp dịch vụ can thiệp này phải có sẵn nhân viên và thiết bị chọc hút màng tim khẩn cấp.
SVC vỡ hoặc thoát mạch ra ngoài màng tim có thể nghiêm trọng không kém, dẫn đến mất máu vào khoang ngực hoặc thành ngực kèm theo hạ huyết áp, tổn thương phổi và tử vong. Các nhà can thiệp và nhân viên phải chuẩn bị sẵn sàng để ứng phó. Duy trì vị trí dây dẫn băng qua vị trí can thiệp là rất quan trọng, để cung cấp bóng chèn ngay vị trí bị gián đoạn để làm hạn chế mất máu. Phẫu thuật khẩn cấp nên được dự phòng trước. Các stent được che phủ hoặc stent có giá đỡ có thể được sử dụng để sửa chữa hoặc đóng vị trí thoát mạch.
Lệch stent có thể xảy ra do làm ngắn stent, hoặc nếu stent được đặt dưới kích thước và có thể được quản lý bằng các kỹ thuật nội mạch như gài trực tiếp stent hoặc gài bóng hỗ trợ có dây dẫn. Tắc stent SVC là một biến chứng muộn và ở bệnh nhân ác tính là do khối u phát triển vào trong hoặc do khối u chèn ép từ bên ngoài.
Ngoài ra, tái hẹp có thể do tăng sản lớp nội mạc hoặc hình thành huyết khối. Đặt stent lặp lại thường có thể có hiệu quả trong việc điều trị tái hẹp hoặc tắc. Phù phổi hiếm gặp và gây ra do sự gia tăng nhanh lưu lượng máu từ tĩnh mạch trở lại sau khi đặt stent. Bệnh nhân có chức năng tim kém dễ mắc hơn và nên được điều trị bằng thuốc lợi tiểu. Việc giám sát sau thủ thuật bao gồm theo dõi lâm sàng chặt chẽ thường 3 tháng một lần và chụp tĩnh mạch lặp lại nếu các triệu chứng tái phát. Bệnh nhân được khuyên tái khám ngay lập tức nếu các triệu chứng tái phát.
9. Triển vọng tương lai
Việc quản lý hội chứng SVC đã phát triển trong 3 thập kỷ qua khi các kỹ thuật can thiệp ngày càng tiến bộ. Tuy nhiên, có rất ít dữ liệu mạnh mẽ và thiếu các hướng dẫn chính thức của xã hội hoặc sự đồng thuận của chuyên gia dành cho các bác sĩ lâm sàng điều trị bệnh nhân bị tắc nghẽn SVC. Cần có các phương pháp chuẩn hóa để phân loại hội chứng SVC, phân loại mức độ nghiêm trọng và hướng dẫn các liệu pháp điều trị. Sự sẵn có của các stent tĩnh mạch và được che phủ chuyên dụng cung cấp nhiều lựa chọn hơn để điều trị cho những bệnh nhân này; vai trò của các thiết bị mới này cần được làm rõ với nhiều kinh nghiệm và bằng chứng hơn.
Các phác đồ chống đông và chống kết tập tiểu cầu tối ưu cho bệnh nhân mắc hội chứng SVC đáng được quan tâm hơn và sẽ chỉ được thiết lập khi thu thập thêm dữ liệu. Hiện nay, đối với các trường hợp tắc nghẽn SVC có huyết khối đáng kể, kháng đông toàn thân là tiêu chuẩn chăm sóc, cả trước và sau khi tái thông mạch. Tuy nhiên, trong trường hợp không có huyết khối đáng chú ý, công dụng của liệu pháp chống đông máu hoặc liêu pháp lấy huyết khối dài hạn vẫn chưa được xác định rõ ràng. Một số người cho rằng chống đông máu toàn thân có thể làm giảm nguy cơ hình thành huyết khối trong stent, trong khi những người khác đề xuất rằng liệu pháp kháng kết hợp tiểu cầu đơn thuần là đủ.
10. Tài liệu tham khảo
- Azizi AH, Shafi I, Shah N, Rosenfield K, Schainfeld R, Sista A, Bashir R. Superior Vena Cava Syndrome. JACC Cardiovasc Interv. 2020 Dec 28;13(24):2896-2910. doi: 10.1016/j.jcin.2020.08.038. PMID: 33357528.
- Lepper PM, Ott SR, Hoppe H, Schumann C, Stammberger U, Bugalho A, Frese S, Schmücking M, Blumstein NM, Diehm N, Bals R, Hamacher J. Superior vena cava syndrome in thoracic malignancies. Respir Care. 2011 May;56(5):653-66. doi: 10.4187/respcare.00947. Epub 2011 Jan 27. PMID: 21276318.
- Akhtar Z, Sohal M, Starck CT, Mazzone P, Melillo F, Gonzalez E, Al-Razzo O, Richter S, Breitenstein A, Steffel J, Rinaldi CA, Mehta V, Zuberi Z, Zaidi A, Gallagher MM. Persistent left superior vena cava transvenous lead extraction: A European experience. J Cardiovasc Electrophysiol. 2022 Jan;33(1):102-108. doi: 10.1111/jce.15290. Epub 2021 Nov 22. PMID: 34783107.
- https://healthjade.net/wp-content/uploads/2019/06/Superior-vena-cava-anatomy.jpg
- https://radiologykey.com/wp-content/uploads/2019/04/f29-01-9781437704075.jpg