Bs. Hoàng Văn Trung
Tóm tắt
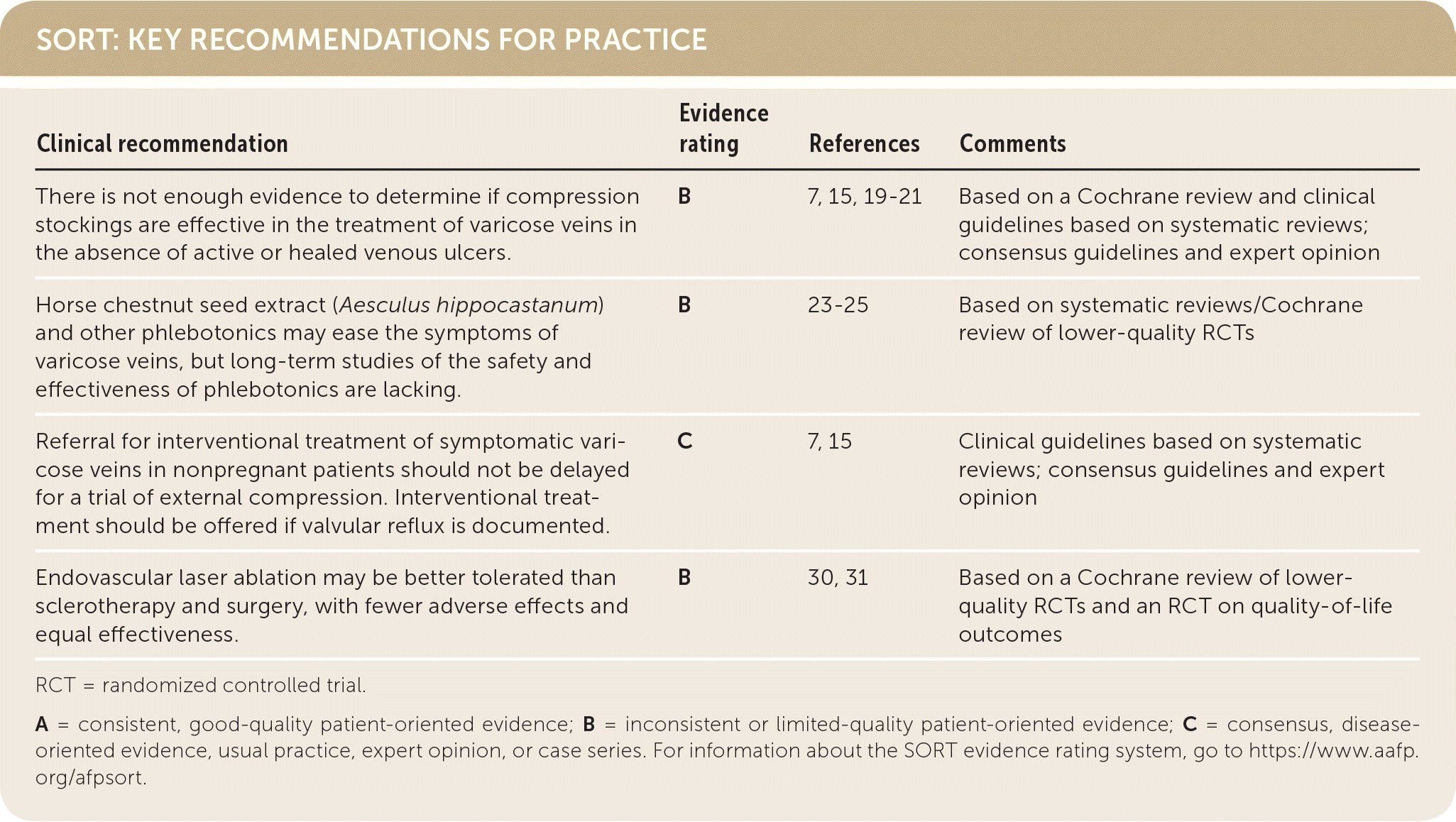
Chứng giãn tĩnh mạch (varicose veins) là sự giãn xoắn ngoằn ngoèo của tĩnh mạch, phổ biến nhất thường ở chi dưới. Sinh lý bệnh chính xác đang được bàn luận, nhưng nó liên quan đến khuynh hướng di truyền, van không đủ chức năng, thành mạch yếu và sự tăng áp lực của tĩnh mạch. Các yếu tố nguy cơ bao gồm tiền sử gia đình mắc bệnh lý tĩnh mạch; giới tính nữ; cao tuổi; tăng áp lực trong ổ bụng mạn tính do béo phì, mang thai, táo bón mạn tính hoặc khối u; và đứng kéo dài. Các triệu chứng của chứng giãn tĩnh mạch bao gồm cảm giác nặng nề, đau nhức và cảm giác ngứa hoặc nóng rát; những triệu chứng xấu đi khi đứng lâu. Các biến chứng tiềm ẩn bao gồm nhiễm trùng, loét chân, ứ máu và huyết khối. Điều trị bảo tồn bao gồm băng ép bên ngoài; điều chỉnh lối sống, chẳng hạn như tránh đứng lâu và tránh căng thẳng mệt mỏi kéo dài, tập thể dục, mặc quần áo không bị gò bó, cải thiện các yếu tố nguy cơ tim mạch và can thiệp để giảm phù ngoại biên; nâng cao chân bị ảnh hưởng; giảm cân; và liệu pháp y học. Không đủ bằng chứng để xác định liệu vớ ép có hiệu quả trong điều trị giãn tĩnh mạch hay không trong trường hợp không có loét tĩnh mạch hoạt động hoặc chữa lành. Các phương pháp điều trị can thiệp bao gồm cắt đốt bằng laser bên ngoài, cắt đốt bằng nhiệt nội mạch, điều trị xơ cứng nội mạch và phẫu thuật. Mặc dù phẫu thuật đã từng là tiêu chuẩn điều trị, nhưng nó phần lớn đã được thay thế bằng phương pháp cắt đốt bằng nhiệt nội mạch, có thể được thực hiện bằng gây tê tại chỗ và có thể có kết quả tốt hơn, ít biến chứng hơn so với các phương pháp điều trị khác. Bằng chứng hiện tại và các hướng dẫn lâm sàng cho thấy rằng một thử nghiệm điều trị nén ép không được bảo đảm trước khi gợi ý cho cắt bỏ bằng nhiệt nội mạch, mặc dù nó có thể cần thiết được bảo đảm.
1. Giới thiệu
Chứng giãn tĩnh mạch là các tĩnh mạch dưới da giãn ra ít nhất 3 mm đường kính khi đo ở tư thế thẳng đứng. Chúng là một phần của quá trình liên tục của các rối loạn tĩnh mạch mạn tính khác nhau, từ giãn tĩnh mạch rõ (telangiectasias), còn được gọi là tĩnh mạch mạng nhện (spider veins, <1 mm) và lưới tĩnh mạch (reticular veins, 1-3 mm) đến suy tĩnh mạch mạn tính (chronic venous insufficiency), có thể bao gồm phù nề , tăng sắc tố và loét tĩnh mạch (Hình 1).
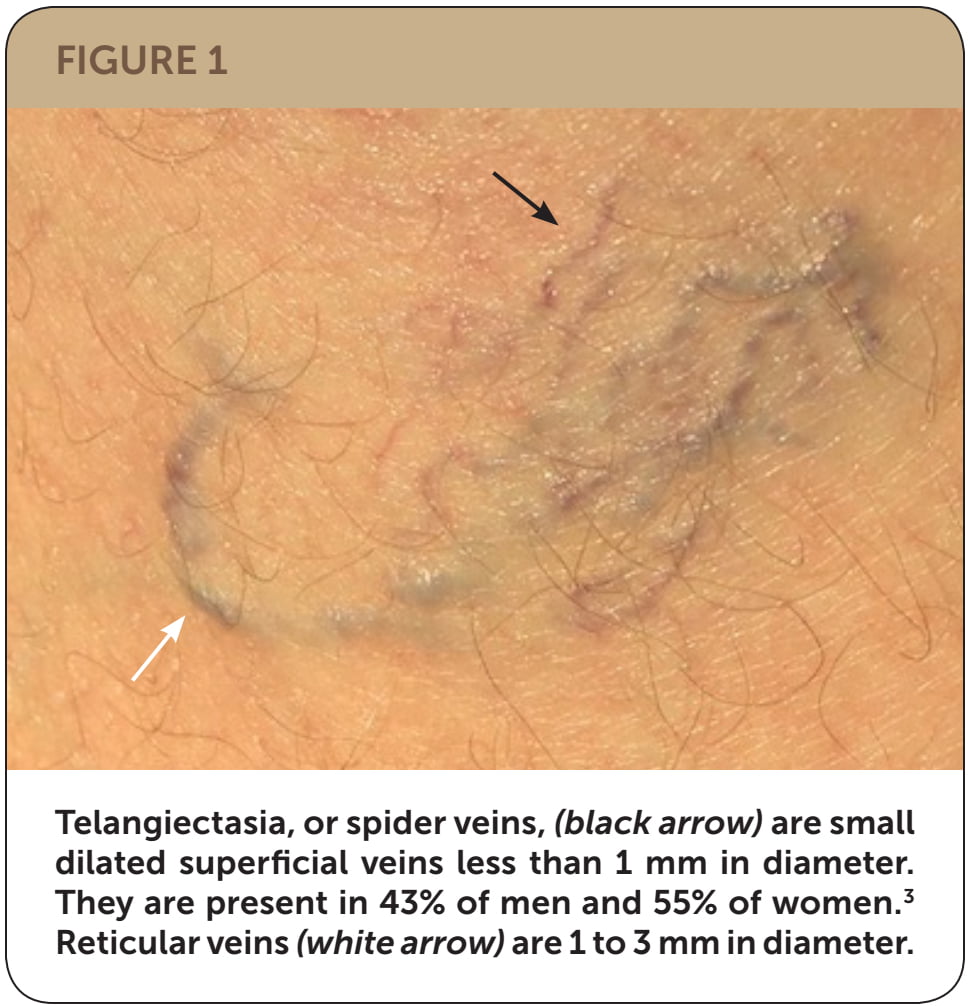
Hình 1. Giãn tĩnh mạch nhỏ hoặc tĩnh mạch mạng nhện (telangiectasia or spider veins, mũi tên đen) là các tĩnh mạch nông nhỏ có đường kính nhỏ hơn 1 mm. Chúng có mặt ở 43% nam giới và 55% nữ giới. Lưới tĩnh mạch (reticular veins, mũi tên trắng) có đường kính từ 1 đến 3 mm.
Bệnh tĩnh mạch mạn tính được mô tả phổ biến nhất bằng cách sử dụng hệ thống phân loại CEAP (clinical, etiologic, anatomic, pathophysiologic – lâm sàng, nguyên nhân, giải phẫu, sinh lý bệnh) (Hình 2). Chứng giãn tĩnh mạch là phổ biến ở chi dưới, với ước tính phổ biến khác nhau. Một nghiên cứu gần đây cho thấy telangiectasias xảy ra ở 43% nam giới và 55% phụ nữ, và suy tĩnh mạch xảy ra ở 16% nam giới và 29% phụ nữ. Trong một dân số có tuổi trung bình là 60, tỷ lệ phân loại CEAP từ C0 đến C6 lần lượt là 29%, 29%, 23%, 10%, 9%, 1.5% và 0.5%.
Hình 2. Hệ thống phân loại cơ bản CEAP của bệnh lý tĩnh mạch mạn tính. Hệ thống phân loại CEAP cung cấp một khung sườn để đặc trưng cho bệnh lý tĩnh mạch, bao gồm cả chứng giãn tĩnh mạch. Phần đầu tiên của hệ thống phân loại CEAP có thể được sử dụng độc lập trong thực tế. Ví dụ, một bệnh nhân đến phòng khám bị giãn tĩnh mạch với phù nhẹ và đau nhưng không nhuộm hemosiderin ở chi dưới có thể được ghi nhận là mắc bệnh tĩnh mạch C3S. Các nghiên cứu tĩnh mạch sẽ là cần thiết để phân loại thêm bệnh nhân bằng cách sử dụng phần còn lại của hệ thống CEAP.
* Sự hiện diện hay vắng mặt của các triệu chứng được ghi nhận với một chỉ số phụ “S” hoặc “A”, ví dụ C1A (telangiectasias không triệu chứng, asymptomatic telangiectasias) hoặc C5S (loét tĩnh mạch đã lành có triệu chứng, symptomatic healed venous ulcer). Các triệu chứng bao gồm đau, nhói, căng, kích ứng da, nặng nề, chuột rút cơ và các triệu chứng khác do rối loạn chức năng tĩnh mạch.
Adapted with permission from Eklöf B, Rutherford RB, Bergan JJ, et al.; American Venous Forum International Ad Hoc Committee for Revision of the CEAP Classification. Revision of the CEAP classification for chronic venous disorders: consensus statement. J Vasc Surg. 2004;40(6):1251–1252.
2. Nguyên nhân
Bệnh lý tĩnh mạch (venous disease) dẫn đến trào ngược van dường như là nguyên nhân cơ bản của chứng giãn tĩnh mạch. Sinh lý bệnh chính xác được tranh luận, nhưng nó liên quan đến khuynh hướng di truyền, van không đủ chức năng, thành mạch máu yếu và tăng áp lực tĩnh mạch. Trong hầu hết các trường hợp, rối loạn chức năng van được cho là do mất tính đàn hồi trong thành tĩnh mạch, với sự thất bại của sự khớp các lá van với nhau. Thay vì máu chảy từ ngoại vi về trung tâm và nông đến sâu, van suy hoặc không đủ khả năng làm máu chảy theo hướng ngược lại. Với áp lực gia tăng lên hệ thống tĩnh mạch bị ảnh hưởng, các tĩnh mạch lớn hơn có thể trở nên dài và quanh co (elongated and tortuous). Căng thẳng gia tăng lên các tế bào nội mô tĩnh mạch do lưu lượng máu đảo ngược hoặc hỗn loạn, và quá trình viêm cũng là những yếu tố căn nguyên quan trọng đối với bệnh llý tĩnh mạch.
Chứng giãn tĩnh mạch ở chân có thể liên quan đến các tĩnh mạch nông quanh trục tĩnh mạch chính (tĩnh mạch hiển lớn và tĩnh mạch hiển bé hoặc các nhánh phụ của chúng). Các yếu tố nguy cơ của chứng suy giãn tĩnh mạch bao gồm tiền sử gia đình mắc bệnh tĩnh mạch; giới tính nữ; tuổi cao hơn; tăng áp lực trong bụng mãn tính do béo phì, mang thai, táo bón mãn tính hoặc khối u; đứng kéo dài; huyết khối tĩnh mạch sâu gây tổn thương van và tái thông mạch máu thứ phát; và dò động tĩnh mạch.
3. Chẩn đoán
Lâm sàng
Biểu hiện lâm sàng của chứng giãn tĩnh mạch là khác nhau, và một số bệnh nhân có thể không có triệu chứng. Các triệu chứng cục bộ có thể là một bên hoặc hai bên bao gồm đau, nóng rát, ngứa và tê rần ở vị trí của tĩnh mạch bị giãn. Các triệu chứng chung bao gồm đau nhức, nặng nề, chuột rút, đau nhói, bồn chồn và sưng ở chân. Các triệu chứng thường tăng nhiều hơn vào cuối ngày, đặc biệt là sau khi đứng lâu và thường hết khi ngồi và nâng cao chân. Phụ nữ có nhiều khả năng có nhiều các triệu chứng ở chi dưới hơn nam giới đã được báo cáo. Bệnh nhân có nhiều khả năng có các triệu chứng và tăng mức độ nghiêm trọng của các triệu chứng khi tăng độ lâm sàng CEAP (C0 đến C6).
Mặc dù chứng giãn tĩnh mạch có thể gây ra mức độ khó chịu hoặc lo ngại về thẩm mỹ khác nhau, nhưng chúng hiếm khi liên quan đến các biến chứng đáng kể. Các dấu hiệu tiềm ẩn của suy mạch máu nghiêm trọng hơn có thể bao gồm thay đổi sắc tố da, chàm, nhiễm trùng, huyết khối tĩnh mạch nông, loét tĩnh mạch, mất mô dưới da và chứng xơ cứng da mỡ (lipodermatosclerosis, giảm chu vi chân do viêm mạn tính, xơ hóa và co rút da và mô dưới da). Mặc dù hiếm, thủng tĩnh mạch gây xuất huyết có ý nghĩa huyết động đã được báo cáo.
Đánh giá các yếu tố nguy cơ, triệu chứng và kết quả khám thực thể điển hình giúp xác định chẩn đoán. Thông qua kiểm tra và sờ nắn, cần lưu ý kích thước và sự phân bố của chứng giãn tĩnh mạch, sự hiện diện và loại phù, và sự hiện diện của sự đổi màu da, lột da hoặc loét. Chứng giãn tĩnh mạch hình quạt (fan-shaped varicose veins) ở mắt cá chân (corona phlebectatica; Hình 3) được coi là một dấu hiệu sớm của bệnh tĩnh mạch tiến triển. Giảm vận động mắt cá chân, mảng da trắng như sẹo (atrophie blanche, một vùng sẹo hình tròn màu trắng bao quanh bởi các mao mạch bị giãn) và chứng xơ cứng da mỡ (lipodermatosclerosis) cũng là dấu hiệu của bệnh tĩnh mạch tiến triển.
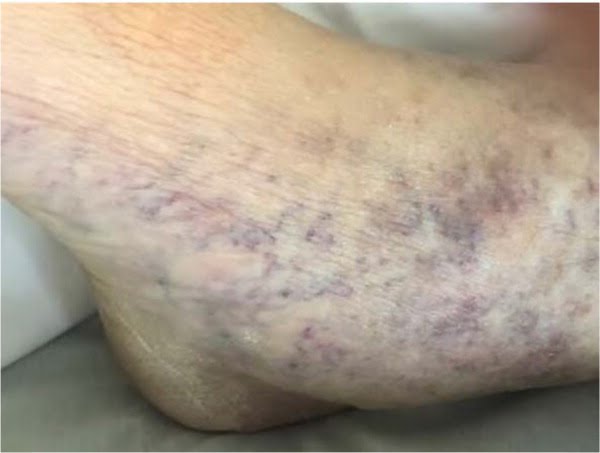
Hình 3. Dấu hiệu giãn tĩnh mạch quanh mắt cá chân (corona phlebectatica) có thể bao gồm các tĩnh mạch màu xanh (blue veins), giãn tĩnh mạch màu xanh (blue telangiectasia), giãn tĩnh mạch màu đỏ (red telangiectasia) và các đốm ứ đọng tối màu (darker stasis spots). Nó được coi là một dấu hiệu sớm của bệnh tĩnh mạch tiến triển. Sử dụng hệ thống phân loại CEAP, bệnh nhân này sẽ được phân loại là mắc bệnh mạch máu C3.
Lưu ý vị trí của các tình trạng giãn tĩnh mạch khác là quan trọng. Giãn tĩnh mạch chậu, âm hộ hoặc háng có thể là một dấu hiệu của sự bất lực hoặc tắc nghẽn tĩnh mạch chậu, có thể bao gồm các khối bụng chậu hoặc thận. Bên cạnh các xét nghiệm lâm sàng được sử dụng để phát hiện vị trí trào ngược, chẳng hạn như sờ nắn một xung truyền ngược từ ngã ba tĩnh mạch hiển-đùi dọc theo tĩnh mạch hiển (tap test) hoặc truyền sự rung động hoặc xung lực tại ngã ba hiển đùi bằng cách cho bệnh nhân ho (cough test). Những phương pháp này có giá trị hạn chế vì độ nhạy hoặc độ đặc hiệu kém.
Hình ảnh học
Khi bệnh lý tĩnh mạch nghiêm trọng hoặc điều trị can thiệp đang được xem xét, siêu âm với chế độ duplex tĩnh mạch là phương thức được lựa chọn. Siêu âm duplex là một phương thức đơn giản, không xâm lấn, không đau và có sẵn để đánh giá giải phẫu và sinh lý của hệ thống tĩnh mạch chi dưới. Nó có thể giúp xác định các chỗ nối của tĩnh mạch hiển không đủ năng lực, đường kính của các chỗ nối, mức độ trào ngược, vị trí và kích thước của các tĩnh mạch xuyên không đủ năng lực khác. Nó cũng có thể đánh giá huyết khối tĩnh mạch sâu cấp tính hoặc bị che khuất, và đánh giá huyết khối tĩnh mạch nông. Trào ngược được định nghĩa là thời gian dòng chảy ngược với hơn 350ms trong các tĩnh mạch xuyên, hơn 500ms trong các tĩnh mạch bề mặt và sâu, và hơn 1s trong các tĩnh mạch vùng kheo đùi (femoropopliteal veins). Các phương thức hình ảnh khác như cắt lớp vi tính, cộng hưởng từ, chụp tĩnh mạch (plethysmography) chỉ được sử dụng nếu siêu âm không kết luận hoặc chuẩn bị cho các tình huống phẫu thuật phức tạp.
4. Điều trị
Việc sử dụng hệ thống phân loại CEAP rất quan trọng để chẩn đoán nhưng không cung cấp hướng dẫn cho các quyết định điều trị. Các lựa chọn điều trị cho chứng giãn tĩnh mạch bao gồm điều trị bảo tồn và các liệu pháp can thiệp như cắt bỏ nhiệt, liệu pháp xơ cứng nội mạch và phẫu thuật (Hình 4).

Hình 4. Các lựa chọn điều trị của chứng giãn tĩnh mạch.
Quyết định tiến hành điều trị và lựa chọn điều trị dựa trên các triệu chứng và sự lựa chọn của bệnh nhân. Những điều quan tâm khác bao gồm chi phí, khả năng biến chứng, nguồn lực sẵn có, bồi hoàn bảo hiểm và đào tạo bác sĩ. Sự hiện diện hoặc vắng mặt của suy tĩnh mạch sâu và đặc điểm của các tĩnh mạch bị ảnh hưởng cũng có thể giúp hướng dẫn điều trị.
Trong 10 năm qua, đã có một sự thay đổi đáng kể trong các khuyến nghị điều trị chúng giãn tĩnh mạch có triệu chứng. Điều này phần lớn là do thiếu bằng chứng hỗ trợ việc sử dụng vớ nén và sự gia tăng của các kỹ thuật nội mạch xâm lấn tối thiểu.
Quản lý thận trọng
Lựa chọn điều trị bảo tồn bao gồm nén ép bên ngoài; sửa đổi lối sống, chẳng hạn như tránh đứng và căng thẳng kéo dài, tập thể dục, mặc quần áo không bị gò bó, điều chỉnh các yếu tố nguy cơ tim mạch và can thiệp để giảm phù ngoại biên; nâng cao chân bị ảnh hưởng; giảm cân; và sử dụng các tác nhân cải thiện hệ tĩnh mạch (phlebotonics). Những biện pháp này được khuyến nghị cho những bệnh nhân chưa cần phải phẫu thuật hoặc điều trị nội mạch, bệnh nhân không muốn can thiệp hoặc đang mang thai.
Nén ép từ lâu đã được khuyến cáo là phương pháp tiếp cận ban đầu cho chứng giãn tĩnh mạch. Tuy nhiên, không có đủ bằng chứng để xác định xem vớ nén có hiệu quả trong điều trị giãn tĩnh mạch trong trường hợp không có loét tĩnh mạch hoạt động hoặc loét đã lành. Hướng dẫn lâm sàng của Viện Sức khỏe và Chăm sóc Quốc gia 2013 (The 2013 National Institute for Health and Care Excellence clinical guidelines) khuyến nghị chỉ yêu cầu nén ép bên ngoài nếu điều trị can thiệp không hiệu quả và chỉ là liệu pháp đầu tay ở phụ nữ mang thai.
Trong một số trường hợp, một thử nghiệm nén ép bên ngoài có thể được yêu cầu bởi các công ty bảo hiểm trước khi phê duyệt phương pháp điều trị can thiệp. Mặc dù chiều dài và áp lực tối ưu để điều trị hiệu quả chưa được xác định, các khuyến nghị điển hình bao gồm mang vớ nén đàn hồi 20-30 mm Hg với độ dốc giảm áp từ phía xa đến đầu gần.
Thuốc cải thiện sức khỏe tĩnh mạch (phlebotonics) là phương pháp điều trị đường uống và dùng tại chỗ có thể làm tăng trương lực tĩnh mạch, cải thiện tình trạng tăng tính thấm mao mạch, và giảm độ nhớt của máu với mục tiêu giảm triệu chứng suy tĩnh mạch mạn tính.
Chúng bao gồm Flavonoid hoặc các hợp chất khác thường được chiết xuất từ thực vật, chẳng hạn như Rutin (còn được gọi là Rutoside), Diosmin, Hidrosmin, Disodium flavodate, chiết xuất vỏ cây thông hàng hải Pháp (Pycnogenol), chiết xuất hạt nho và hạt dẻ ngựa (Aesculus hippocastanum). Diosmiplex (Vasculera) là công thức kê đơn duy nhất có sẵn ở Hoa Kỳ. Diosmiplex có nguồn gốc từ vỏ cam và được phân loại là thực phẩm chức năng, không phải là thuốc. Liều dùng thông thường là 630 mg mỗi ngày.
Chiết xuất hạt dẻ ngựa dường như an toàn và hiệu quả trong việc giảm đau, giảm phù và ngứa do suy tĩnh mạch mạn tính khi sử dụng trong 2 đến 16 tuần. Liều dùng phổ biến là 300 mg hai lần mỗi ngày hoặc 50 mg Aescin. Có bằng chứng có chất lượng vừa phải cho thấy các chất cải thiện tĩnh mạch khác có thể giảm chứng phù và giảm các triệu chứng như chuột rút, chân không yên và dị cảm.
Hầu hết các chất cải thiện tĩnh mạch có sẵn dưới dạng thực phẩm bổ sung ở Hoa Kỳ, và nhiều công thức có chứa đa chất trong một công thức duy nhất. Các nghiên cứu dài hạn về sự an toàn và hiệu quả của chất cải thiện tĩnh mạch trong điều trị suy tĩnh mạch là vẫn còn thiếu.
Điều trị can thiệp
Đốt bằng nhiệt (Thermal ablation)
Sự đốt bằng nhiệt phá hủy các tĩnh mạch bị tổn thương bằng cách sử dụng tia laser bên ngoài hoặc sử dụng tia laser nội mạch qua ống thông (endovenous laser ablation – cắt đốt bằng laser nội mạch) hoặc đốt bằng sóng cao tần (radiofrequency ablation, đốt bằng nhiệt sử dụng sóng cao tần). Cắt đốt bằng laser bên ngoài hoạt động tốt nhất cho telangiectasias. Trong liệu pháp này, huyết sắc tố (hemoglobin) hấp thụ ánh sáng laser dẫn đến quá trình nhiệt hóa. Đốt nhiệt nội mạch có thể được sử dụng cho các mạch máu lớn hơn, bao gồm cả tĩnh mạch hiển lớn. Dưới hướng dẫn siêu âm, một điện cực (catheter electrode) với sợi laser quang học (laser optical fiber) hoặc sóng cao tần (radiofrequency) được đưa vào tĩnh mạch theo hướng từ xa đến gần. Nhiệt từ tia laser hoặc sóng vô tuyến làm đông máu trong tĩnh mạch, dẫn đến làm tắc tĩnh mạch và chuyển hướng dòng máu đến các tĩnh mạch có chức năng.
Liệu pháp gây xơ hóa nội tĩnh mạch (Endovenous sclerotherapy)
Liệu pháp gây xơ hóa nội tĩnh mạch liên quan đến việc sử dụng siêu âm hướng dẫn để vào các tĩnh mạch bề mặt với một tác nhân gây cháy nội mạc, dẫn đến xơ hóa và bít tắc lòng tĩnh mạch. Điều trị xơ hóa thường được sử dụng cho các tĩnh mạch nhỏ (1-3 mm) và tĩnh mạch trung bình (3-5 mm) hoặc để điều trị chứng giãn tĩnh mạch tái phát sau phẫu thuật; tuy nhiên, không có một đường kính chính xác được sử dụng để đưa ra quyết định điều trị.
Một cây kim được đưa vào trong lòng tĩnh mạch và tác nhân gây xơ hóa được tiêm vào, thường có không khí để tạo bọt. Bọt sẽ thay thế máu và phản ứng với nội mô mạch máu, bít kín và hình thành sẹo tĩnh mạch. Một loạt các tác nhân có thể được sử dụng, bao gồm nước muối ưu trương, natri tetradecyl (Sotradecol) và polidocanol (Varithena). Không có bằng chứng cho thấy bất kỳ tác nhân nào trong số này là vượt trội so với các tác nhân khác về hiệu quả hoặc sự hài lòng của bệnh nhân.
Phẫu thuật (Surgery)
Trong lịch sử, phẫu thuật thắt (ligation) và tước tĩnh mạch (stripping) hiển lớn hoặc hiển bé là tiêu chuẩn để điều trị chứng giãn tĩnh mạch sau thất bại của liệu pháp bảo tồn. Tuy nhiên, một số tài liệu không đồng tình với quan điểm hỗ trợ phẫu thuật là lựa chọn điều trị can thiệp tốt nhất, và hướng dẫn lâm sàng của Viện Sức khỏe và Chăm sóc Quốc gia 2013 khuyến nghị phẫu thuật là liệu pháp thứ ba sau đốt nội tĩnh mạch và điều trị xơ hóa.
Các kỹ thuật phẫu thuật cập nhật sử dụng các vết mổ nhỏ để giảm sẹo, giảm mất máu và các biến chứng, hạn chế loại bỏ các tĩnh mạch nông quanh trục từ háng đến đầu gối. Một số các thủ tục này có thể được thực hiện dưới gây tê vùng hoặc gây mê. Thắt và tước tĩnh mạch hiển lớn và bé có lẽ là thủ tục được biết đến nhiều nhất. Thông thường, tĩnh mạch được cắt ở đầu gần, một tĩnh mạch được tước tới vết mổ ở đầu xa nằm ở gần đầu gối để tiếp cận với một đầu của sợi stripper. Đầu tận cùng của sợi stripper được xuyên vào tĩnh mạch và tĩnh mạch sau đó được lấy ra khi sợi stripper được kéo ra xa. Các tĩnh mạch không phải hiển lớn và hiển bé có thể được loại bỏ thông qua phẫu thuật cắt bỏ tĩnh mạch, trong đó sử dụng dao mổ hoặc kim có kích thước lớn để tạo ra các vết thủng mỗi 2 đến 3 cm dọc theo tĩnh mạch giãn. Các đoạn của tĩnh mạch bị hư hỏng được loại bỏ bằng kẹp hoặc móc nhỏ.
Dữ liệu kết quả
Một tổng quan của Cochrane năm 2014 đã kết luận rằng đốt laser nội mạch, đốt bằng sóng cao tần và điều trị xơ cứng bằng bọt có hiệu quả tương đương với phẫu thuật trong điều trị chứng giãn tĩnh mạch hiển lớn. Các tài liệu trước đây cho rằng điều trị phẫu thuật truyền thống của chứng giãn tĩnh mạch với thắt tĩnh mạch lớn ở ngã ba hiển đùi và tước tĩnh mạch có tỷ lệ tái phát trong 5 năm khoảng 20-28%. Tái phát lâm sàng của chứng giãn tĩnh mạch sau 5 năm được đo chỉ trong một nghiên cứu trong tổng quan của Cochrane và cho thấy không có sự khác biệt giữa đốt bằng laser nội mạch và phẫu thuật. Duy trì tắc nghẽn tĩnh mạch hiển lớn sau 6 tháng với điều trị xơ cứng ít hơn so với phẫu thuật hoặc đốt laser nội mạch (43% so với 80%). Đốt bằng nhiệt ít tái phát trào ngược sau một năm so với phẫu thuật khi điều trị chứng giãn tĩnh mạch của tĩnh mạch hiển bé đưa đến từ sự bất lực của khớp nối hiển khoeo.
Các liệu pháp không phẫu thuật có thể có thời gian hồi phục và làm việc nhanh hơn so với phẫu thuật. Cắt đốt bằng laser nội mạch có thể được dung nạp tốt hơn so với liệu pháp xơ cứng và phẫu thuật, với ít tác dụng phụ hơn và hiệu quả tương đương. Đối với cả ba phương pháp điều trị, tỷ lệ biến chứng nhỏ và lớn, bao gồm tê, bầm tím hoặc đau dai dẳng, loét da, nhuộm da và sần da tương đối thấp (1 đến 7%). Máu tụ xảy ra thường xuyên với điều trị phẫu thuật hơn so với điều trị xơ cứng bằng bọt hoặc đốt cao tần. Cắt đốt bằng laser nội mạch dường như vượt trội hơn so với phẫu thuật về sự thất bại kỹ thuật và sự tân tạo mạch. Mặc dù tất cả các phương pháp điều trị can thiệp đều dẫn đến cải thiện triệu chứng, sự cải thiện sau 6 tháng có thể có ý nghĩa đối với phẫu thuật và đốt laser nội mạch hơn so với liệu pháp gây xơ cứng bằng bọt.
5. Tài liệu tham khảo
1. Eklöf B, Rutherford RB, Bergan JJ, et al.; American Venous Forum International Ad Hoc Committee for Revision of the CEAP Classification. Revision of the CEAP classification for chronic venous disorders: consensus statement. J Vasc Surg. 2004;40(6):1248–1252.
2. Eberhardt RT, Raffetto JD. Chronic venous insufficiency. Circulation. 2014;130(4):333–346.
3. Kaplan RM, Criqui MH, Denenberg JO, Bergan J, Fronek A. Quality of life in patients with chronic venous disease: San Diego population study. J Vasc Surg. 2003;37(5):1047–1053.
4. McLafferty RB, Passman MA, Caprini JA, et al. Increasing awareness about venous disease: The American Venous Forum expands the National Venous Screening Program. J Vasc Surg. 2008;48(2):394–399.
5. Clarke GH, Vasdekis SN, Hobbs JT, Nicolaides AN. Venous wall function in the pathogenesis of varicose veins. Surgery. 1992;111(4):402–408.
6. Bergan JJ, Schmid-Schönbein GW, Smith PD, Nicolaides AN, Boisseau MR, Eklof B. Chronic venous disease. N Engl J Med. 2006;355(5):488–498.
7. Gloviczki P, Comerota AJ, Dalsing MC, et al. The care of patients with varicose veins and associated chronic venous diseases: clinical practice guidelines of the Society for Vascular Surgery and the American Venous Forum. J Vasc Surg. 2011;53(5 suppl):2S–48S.
8. Beebe-Dimmer JL, Pfeifer JR, Engle JS, Schottenfeld D. The epidemiology of chronic venous insufficiency and varicose veins. Ann Epidemiol. 2005;15(3):175–184.
9. Sadick NS. Advances in the treatment of varicose veins: ambulatory phlebectomy, foam sclerotherapy, endovascular laser, and radiofrequency closure. Dermatol Clin. 2005;23(3):443–455, vi.
10. Teruya TH, Ballard JL. New approaches for the treatment of varicose veins. Surg Clin North Am. 2004;84(5):1397–1417, viii–ix.
11. Langer RD, Ho E, Denenberg JO, Fronek A, Allison M, Criqui MH. Relationships between symptoms and venous disease: the San Diego population study. Arch Intern Med. 2005;165(12):1420–1424.
12. Bradbury A, Evans C, Allan P, Lee A, Ruckley CV, Fowkes FG. What are the symptoms of varicose veins? Edinburgh vein study cross sectional population survey. BMJ. 1999;318(7180):353–356.
13. Racette S, Sauvageau A. Unusual sudden death: two case reports of hemorrhage by rupture of varicose veins. Am J Forensic Med Pathol. 2005;26(3):294–296.
14. Kim J, Richards S, Kent PJ. Clinical examination of varicose veins—a validation study. Ann R Coll Surg Engl. 2000;82(3):171–175.
15. National Institute for Health and Care Excellence. Varicose veins: diagnosis and management. Clinical guideline 168. July 2013. https://www.nice.org.uk/guidance/cg168. Accessed May 21, 2018.
16. Labropoulos N, Tiongson J, Pryor L, et al. Definition of venous reflux in lower-extremity veins. J Vasc Surg. 2003;38(4):793–798.
17. Coleridge-Smith P, Labropoulos N, Partsch H, Myers K, Nicolaides A, Cavezzi A. Duplex ultrasound investigation of the veins in chronic venous disease of the lower limbs—UIP consensus document. Part I. Basic principles. Eur J Vasc Endovasc Surg. 2006;31(1):83–92.
18. Jones RH, Carek PJ. Management of varicose veins. Am Fam Physician. 2008;78(11):1289–1294.
19. Shingler S, Robertson L, Boghossian S, Stewart M. Compression stockings for the initial treatment of varicose veins in patients without venous ulceration. Cochrane Database Syst Rev. 2013;(12):CD008819.
20. O’Meara S, Cullum N, Nelson EA, Dumville JC. Compression for venous leg ulcers. Cochrane Database Syst Rev. 2012;(11):CD000265.
21. Nelson EA, Bell-Syer SE. Compression for preventing recurrence of venous ulcers. Cochrane Database Syst Rev. 2014;(9):CD002303.
22. Lam Ey, Giswold ME, Moneta GL. Venous and lymphatic disease. In: Dries DJ, ed. Schwartz’s Principles of Surgery. 8th ed. New York, NY: McGraw-Hill; 2005:823–825.
23. Bush R, Comerota A, Meissner M, Raffetto JD, Hahn SR, Freeman K. Recommendations for the medical management of chronic venous disease: the role of micronized purified flavonoid fraction (MPFF) [published correction appears in Phlebology. 2017;32(10):NP36]. Phlebology. 2017;32(1 suppl):3–19.
24. Pittler MH, Ernst E. Horse chestnut seed extract for chronic venous insufficiency. Cochrane Database Syst Rev. 2012;(11):CD003230.
25. Martinez-Zapata MJ, Vernooij RW, Uriona Tuma SM, et al. Phlebotonics for venous insufficiency. Cochrane Database Syst Rev. 2016;(4):CD003229.
26. Reichert D. Evaluation of the long-pulse dye laser for the treatment of leg telangiectasias. Dermatol Surg. 1998;24(7):737–740.
27. Paravastu SC, Horne M, Dodd PD. Endovenous ablation therapy (laser or radiofrequency) or foam sclerotherapy versus conventional surgical repair for short saphenous varicose veins. Cochrane Database Syst Rev. 2016;(11):CD010878.
28. Tisi PV, Beverley C, Rees A. Injection sclerotherapy for varicose veins. Cochrane Database Syst Rev. 2006;(4):CD001732.
29. Schwartz L, Maxwell H. Sclerotherapy for lower limb telangiectasias. Cochrane Database Syst Rev. 2011;(12):CD008826.
30. Nesbitt C, Bedenis R, Bhattacharya V, Stansby G. Endovenous ablation (radiofrequency and laser) and foam sclerotherapy versus open surgery for great saphenous vein varices. Cochrane Database Syst Rev. 2014;(7):CD005624.
31. Brittenden J, Cotton SC, Elders A, et al. A randomized trial comparing treatments for varicose veins. N Engl J Med. 2014;371(13):1218–1227.
Nguồn: Jaqueline A, Megan W, Kimberly C. Varicose Veins: Diagnosis and Treatment; Am Fam Physician. 2019 Jun 1;99(11):682-688. aafp.org/afp/2019/0601/p682