Mục lục bài viết
- 1. Giới thiệu
- 2. Danh sách báo cáo kết quả
- 3. Hình thái học
- 4. Vị trí
- 5. Giai đoạn T
- 5.1. T1-T2 – giới hạn ở thành ruột
- 5.2. T3 – xâm lấn vào lớp mỡ mạc treo trực tràng
- 5.3. Liên quan đến cân mạc treo trực tràng (Mesorectal fascia involvement)
- 5.4. Cân mạc treo trực tràng và phúc mạc (Mesorectal fascia versus Peritoneum)
- 5.5. T4a – Xâm lấn phúc mạc hoặc chỗ quặt ngược phúc mạc
- 5.6. T4b – Xâm lấn các cơ quan hoặc cấu trúc xung quanh
- 5.7. Nhận ra giai đoạn xâm lấn T4b
- 5.8. EMVI – Xâm lấn mạch máu ngoài thành (Extramural vascular invasion)
- 5.9. Liên quan cơ vòng hậu môn và sàn chậu
- 6. Giai đoạn N
- 7. Giai đoạn M
- 8. Đánh giá lại sau điều trị bổ trợ
- 9. MRI protocol
- 10. Phẫu thuật
- 10.1. Phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng (Total mesorectal excision)
- 10.2. Phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng (Low anterior resection)
- 10.3. Cắt cụt trực tràng qua đường bụng- tầng sinh môn (Abdominoperineal resection)
- 10.4. Cắt cụt trực tràng qua ngả bụng tầng sinh môn trong cơ thắt (Intersphincteric abdomino perineal resection)
- 10.5. Cắt cụt trực tràng qua ngả bụng tầng sinh môn ngoài cơ nâng hậu môn (Extralevator abdomino-perineal resection)
- 10.6. Cắt bỏ cục bộ
- 11. Nguồn
1. Giới thiệu
1.1. Cắt bỏ toàn bộ mạc treo trực tràng
Hai tiến bộ chính trong điều trị ung thư trực tràng là phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng và xạ trị bổ trợ có hoặc không hóa trị liệu. Cả hai đều đã làm thay đổi đáng kể tỷ lệ tái phát và sống sót tại chỗ.
MRI là công cụ chính xác nhất để xác định giai đoạn cục bộ của ung thư trực tràng và là một công cụ mạnh để giúp lựa chọn phương pháp điều trị thích hợp. Việc xem xét bệnh nhân bị ung thư trực tràng nên điều trị phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng hay liệu pháp bổ trợ trước khi phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng sẽ được quyết định dựa trên kết quả của MRI.
Trong phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng, toàn bộ khoang mạc treo trực tràng bao gồm trực tràng, lớp mỡ xung quanh mạc treo trực tràng và các hạch bạch huyết quanh trực tràng được loại bỏ hoàn toàn dọc theo cân mạc treo trực tràng. Phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng là kỹ thuật cắt bỏ tiêu chuẩn đối với ung thư trực tràng và có thể được thực hiện như một phương pháp cắt bỏ trước thấp (LAR) nơi ống hậu môn được giữ lại tại chỗ hoặc phương pháp cắt cụt trực tràng qua đường bụng – tầng sinh môn (APR), trong đó cả trực tràng và ống hậu môn đều bị cắt bỏ.
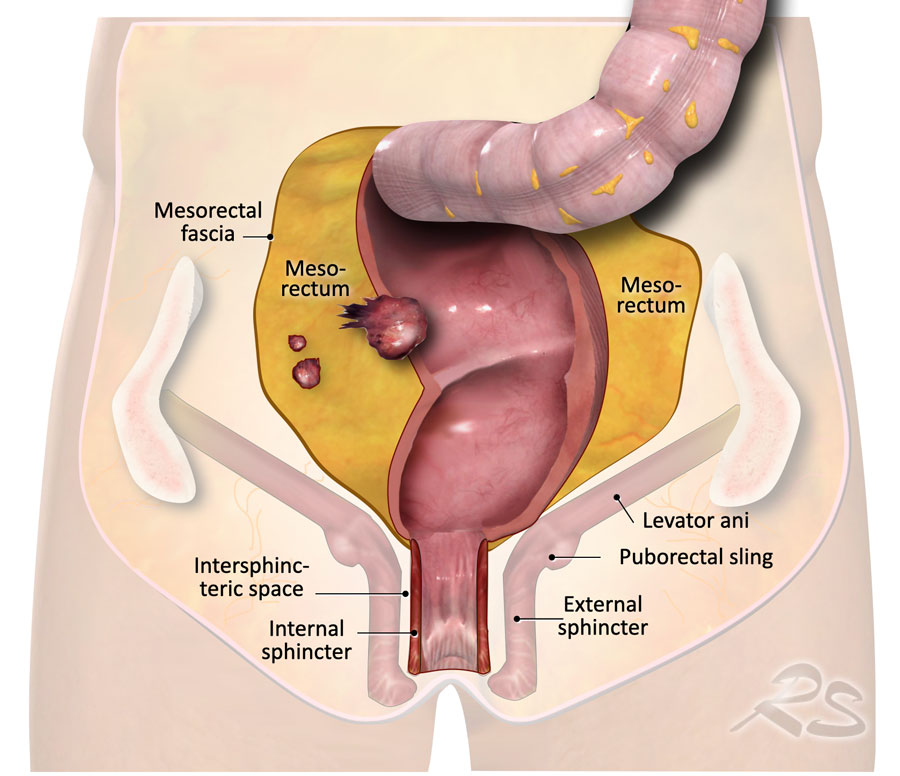
Hình 1. Hình minh họa cho thấy mạc treo trực tràng và cân mạc treo trực tràng, là mặt phẳng để phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng và mối liên hệ của trực tràng với cơ thắt hậu môn và sàn chậu.
1.2. Phân cấp rủi ro
Phân giai đoạn cục bộ trên MRI được thực hiện để xác định chiến lược phẫu thuật tốt nhất và xem xét sự cần thiết của điều trị bổ trợ.
Các tiêu chí được sử dụng để xác định nguy cơ thấp, nguy cơ trung bình, và nguy cơ cao; và việc sử dụng chúng để phân tầng điều trị khác nhau giữa các quốc gia và giữa các hướng dẫn và chúng đang liên tục được phát triển. Theo nguyên tắc chung, chúng ta có thể nêu ra như sau:
Nguy cơ thấp
T1, T2 và ở một số quốc gia cũng có khối u giai đoạn sớm T3ab mà không có bằng chứng về di căn hạch nói chung sẽ được coi là nguy cơ thấp và không nhất thiết phải điều trị bổ trợ.
Nguy cơ trung bình
Các khối u T3 mở rộng hơn và / hoặc các khối u có số lượng hạn chế các hạch nghi ngờ thường được coi là nguy cơ trung bình. Một đợt xạ trị ngắn (5 x 5 Gy) trước phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng đã được chứng minh là làm giảm nguy cơ tái phát cục bộ đối với các khối u nguy cơ trung bình này.
Nguy cơ cao hoặc tiến triển cục bộ
Các khối u T3-4 tiến triển xâm lấn vào cân mạc treo trực tràng hoặc các cơ quan lân cận, hoặc các khối u có nhiều hạch nghi ngờ (N2) thường được coi là tiến triển cục bộ. Những trường hợp này thường cần một đợt hóa trị liệu kết hợp kéo dài nhằm mục đích làm giảm kích thước và hạ thấp giai đoạn khối u, và nâng cao cơ hội phẫu thuật cắt bỏ hoàn toàn. Gần đây hơn, sự hiện diện của xâm lấn mạch máu ngoài thành (hoặc tĩnh mạch) đã được đề xuất như một đặc điểm tiên lượng bất lợi bổ sung và nên được coi là một dấu hiệu của nguy cơ cao.
 Hình 2. Tiêu chí phân tầng điều trị
Hình 2. Tiêu chí phân tầng điều trị
Ngày càng có xu hướng xem xét các lựa chọn thay thế điều trị xâm lấn tối thiểu hoặc điều trị không phẫu thuật đối với các khối u cho thấy đáp ứng hoàn toàn hoặc gần hoàn toàn sau khi điều trị bổ trợ. MRI đóng một vai trò quan trọng ngoài nội soi để giúp định hướng đúng các phương pháp điều trị “bảo tồn nội tạng” này.
Ngoài việc bảo tồn nội tạng, những tiến bộ gần đây trong điều trị bao gồm:
-Phát triển các phương pháp bổ trợ trị liệu mới như kết hợp hóa trị liệu kéo dài với xạ trị liệu trình ngắn
-Chiến lược tăng cường xạ trị
-Liệu pháp miễn dịch
-Phát triển trong kỹ thuật cắt bỏ tại chỗ và xạ trị tại chỗ đối với các khối u giai đoạn đầu hoặc khối u nhỏ còn sót lại sau bổ trợ trị liệu
2. Danh sách báo cáo kết quả

Hình 3. Mẫu mô tả báo cáo hình ảnh
Một báo cáo MRI chất lượng tốt bao gồm tất cả các yếu tố nguy cơ được sử dụng để phân tầng bệnh nhân thành các phương pháp điều trị khác nhau, cũng như mô tả chính xác về mối quan hệ của khối u với giải phẫu xung quanh nó để đưa ra kế hoạch phẫu thuật.
Tiền tố TNM
“c” được sử dụng để chỉ giai đoạn lâm sàng, được xác định trước khi điều trị. Khi được xác định dựa trên hình ảnh, tiền tố “i” (hình ảnh) hoặc “mr” (MRI) đôi khi được sử dụng làm lựa chọn thay thế.
“y” được sử dụng để phân độ lại khối u sau khi điều trị bổ trợ (hóa trị và / hoặc xạ trị) và có thể được sử dụng cho cả giai đoạn lâm sàng (ycTNM) cũng như giai đoạn bệnh lý (ypTNM).
“p” chỉ giai đoạn TNM cuối cùng được xác định ở mô bệnh học sau phẫu thuật.
3. Hình thái học
3.1. Khối u có cuống và không cuống
Ung thư biểu mô tuyến trực tràng thường phát sinh từ các u tuyến có thể là polyp, là những khối u có cuống hoặc không cuống. Các khối u dạng polyp thường đại diện cho các khối u ác tính grade thấp hơn và biểu hiện dưới dạng một khối lồi vào lòng ruột với một đầu đính vào thành ruột hoặc có cuống đính vào thành ruột. Các khối u không cuống thường biểu hiện dưới dạng dày thành hình bán nguyệt hoặc theo chu vi. Vị trí mà khối u bám vào thành trực tràng thường được gọi là bờ xâm lấn và là vị trí mà chúng ta cần tập trung khi đánh giá giai đoạn T và tìm kiếm sự mở rộng của khối u ra ngoài thành.
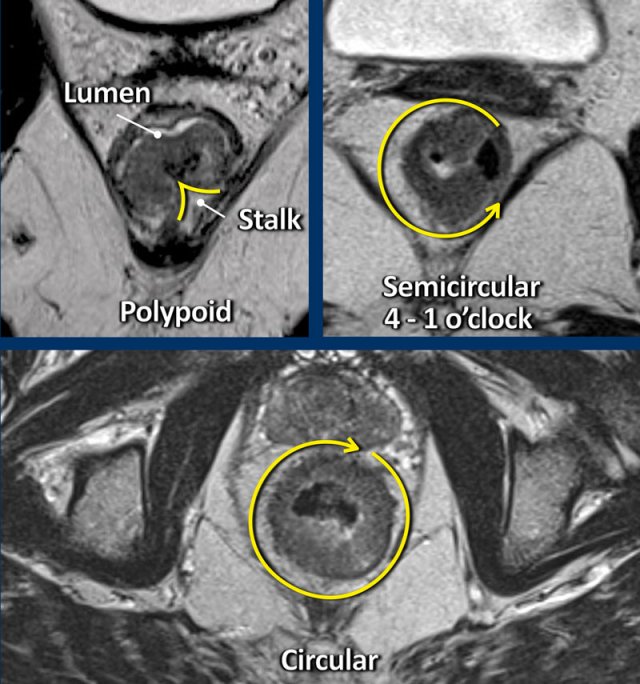
Hình 4. Mức độ đính vào thành trực tràng, còn được gọi là chu vi khối u, có thể được mô tả trong báo cáo chẩn đoán hình ảnh như “từ vị trí mấy giờ đến vị trí mấy giờ”, hoặc cách khác sử dụng các mô tả chung chẳng hạn như “vị trí trước bên bên trái”.
3.2. Đặc hoặc nhầy
Sự phân biệt giữa các loại khối u đặc và u nhầy là có liên quan bởi vì ung thư biểu mô tuyến nhầy có tiên lượng kém hơn và thường cho thấy đáp ứng kém hơn với điều trị bổ trợ. Các khối u nhầy cho thấy tín hiệu sáng rõ ràng trên T2W so với tín hiệu trung gian của các khối u đặc.
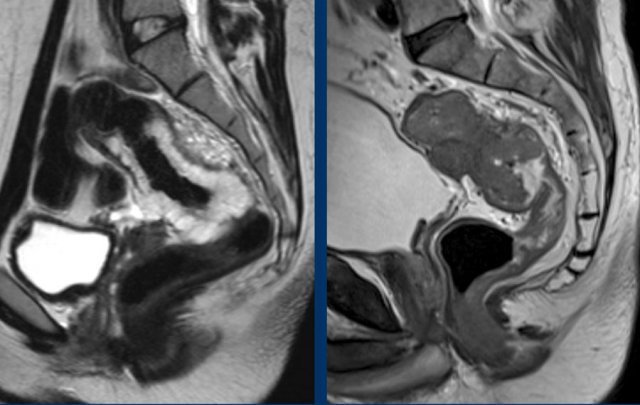
Khối u nhầy sáng so với khối u đặc có tín hiệu trung gian.
3.3. Ung thư biểu mô tế bào signet-ring
Một loại phụ hiếm gặp hơn của ung thư trực tràng là ung thư biểu mô tế bào signet-ring, có liên quan đến nguy cơ cao đối với di căn xa và di căn hạch, và khả năng sống tổng thể kém. Nó chỉ được nhìn thấy trong khoảng một phần trăm các trường hợp. Trên MRI, ung thư tế bào signet-ring có thể khó nhận biết, mặc dù chúng thường cho thấy dày thành ruột lan tỏa một đoạn dài và có mô hình phát triển dưới niêm mạc dẫn đến xuất hiện ‘dấu bia bắn’ trên các hình ảnh axial.
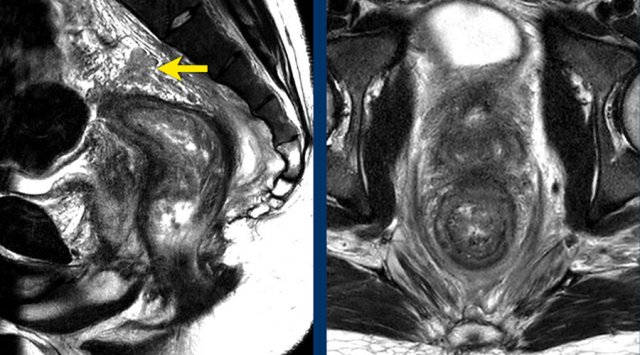 Hình 5. Hình ảnh cho thấy ung thư biểu mô tế bào signet-ring với sự dày lên lan tỏa của thành trực tràng và xuất hiện hình ảnh bia bắn trên hình ảnh axial. Cũng cần lưu ý đến sự thâm nhiễm lan tỏa của mỡ mạc treo trực tràng, đây là một phát hiện phổ biến khác của các khối u tế bào signet-ring.
Hình 5. Hình ảnh cho thấy ung thư biểu mô tế bào signet-ring với sự dày lên lan tỏa của thành trực tràng và xuất hiện hình ảnh bia bắn trên hình ảnh axial. Cũng cần lưu ý đến sự thâm nhiễm lan tỏa của mỡ mạc treo trực tràng, đây là một phát hiện phổ biến khác của các khối u tế bào signet-ring.
4. Vị trí
4.1. Ranh giới đại tràng sigma (Sigmoid take-Off)
Phân biệt ung thư trực tràng với ung thư đại tràng là rất quan trọng vì phương pháp điều trị khác nhau đáng kể. Điều trị thường quy đối với ung thư đại tràng sigma là cắt bỏ trước trên, trong khi các khối u trực tràng trải qua các phương pháp điều trị khác nhau, từ phẫu thuật ở các khối u nguy cơ thấp đến hóa xạ trị bổ trợ dài hạn ở các khối u nguy cơ cao.
Vào năm 2019, một hội đồng đồng thuận quốc tế đã đồng ý dùng “sigmoid take-off” làm mốc ưa thích để xác định chỗ nối trực tràng và đại tràng sigma.
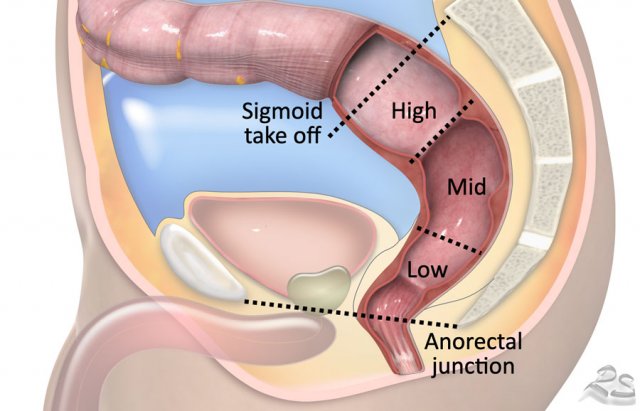 Hình 6. Sigmoid take-off có thể được nhận ra trên MRI sagittal là điểm mà từ đó đại tràng sigma quét theo chiều ngang ra khỏi xương cùng và trên hình chiếu axial là điểm mà từ đó sigmoid đi vào bụng.
Hình 6. Sigmoid take-off có thể được nhận ra trên MRI sagittal là điểm mà từ đó đại tràng sigma quét theo chiều ngang ra khỏi xương cùng và trên hình chiếu axial là điểm mà từ đó sigmoid đi vào bụng.
Mặc dù việc nhận biết sigmoid take-off trên hình ảnh có thể là một thách thức trong một số trường hợp do sự khác biệt về giải phẫu giữa các bệnh nhân hoặc sự thay đổi góc của các chuỗi xung, nhưng nhìn chung đây là một mốc theo cảm tính. Các khối u ở trên mức chỗ nối trực tràng và đại tràng sigma với bờ dưới bắt đầu từ sigmoid take-off được coi là khối u đại tràng sigma.
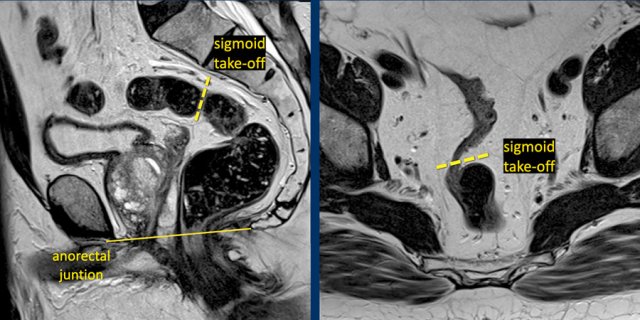
Hình 7. Đường cố định cho biết sigmoid take-off trên mặt phẳng sagittal và axial
4.2. Chiều cao khối u
Chỗ nối hậu môn trực tràng (anorectal junction marks) đánh dấu sự chuyển tiếp giữa ống hậu môn và đoạn xa trực tràng. Nó nằm ở mức của góc hậu môn trực tràng (anorectal angle), được tạo ra do sự co thắt của cơ mu trực tràng (puborectalis muscle). Trên MRI sagittal, điểm nối hậu môn trực tràng thường nằm ở mức của đường tưởng tượng giữa bờ dưới của xương cùng (sacral bone) và xương mu (pubic bone).
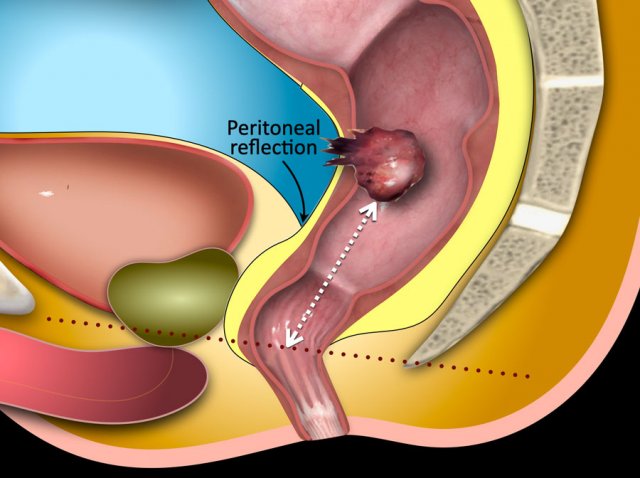
Hình 8. Cách tiếp cận phổ biến để xác định chiều cao của khối u trực tràng là đo khoảng cách giữa bờ dưới của khối u và chỗ nối hậu môn trực tràng
Một cách khác là đo khoảng cách từ bờ hậu môn (anal verge), là nơi chuyển tiếp giữa biểu mô hậu môn (anal epithelium) và da quanh hậu môn (perianal skin). Ở một số nước như Mỹ, vị trí của khối u liên quan đến chỗ quặt ngược phía trước của phúc mạc thường được dùng làm mốc để xác định chiều cao khối u.
5. Giai đoạn T
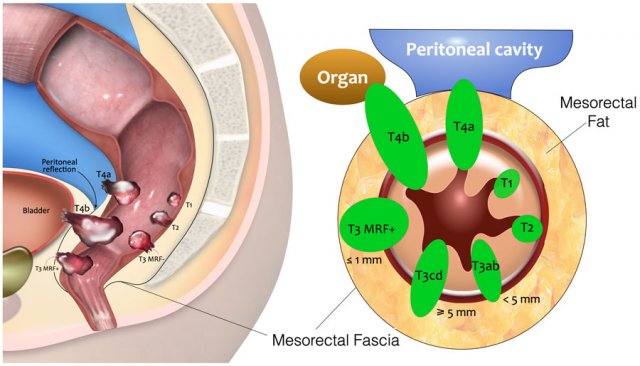
Hình 9. Hình minh họa các giai đoạn T trong mặt phẳng sagittal và mặt phẳng axial.
-Các khối u T1 chỉ xâm lấn lớp dưới niêm mạc (submucosa).
-Các khối u T2 xâm lấn lớp đệm cơ (muscularis propria), là lớp cơ bên ngoài của thành trực tràng.
-Các khối u T3 phát triển vào vào lớp mỡ mạc treo trực tràng
-Các khối u T3 MRF- chưa phát triển đến cân mạc treo trực tràng (MRF – mesorectal fascia).
-Các khối u T3 MRF+ xâm lấn vào cân mạc treo trực tràng hoặc có rìa ≤1mm tính từ cân mạc treo trực tràng.
-Các khối u T4a xâm lấn phúc mạc hoặc chỗ quặt ngược phúc mạc.
-Các khối u T4b xâm lấn các cơ quan hoặc cấu trúc khác bên ngoài lớp mạc treo trực tràng.
 Hình 10. Hình mô tả tổng quan về hệ thống phân loại T.
Hình 10. Hình mô tả tổng quan về hệ thống phân loại T.
-Các khối u T3 có nguy cơ thấp có sự mở rộng tối thiểu vào lớp mỡ mạc treo trực tràng lên đến 5mm (T3ab) và không liên quan đến cân mạc treo trực tràng (khoảng cách ≥1mm).
-Các khối u T3 có nguy cơ cao mở rộng vào lớp mỡ mạc treo trực tràng >5mm hoặc xâm lấn vào cân mạc treo trực tràng.
-Các khối u T4b xâm lấn các cơ quan hoặc cấu trúc khác nằm bên ngoài mạc treo trực tràng.
Hệ thống phân loại TNM không bao gồm mô tả rõ ràng về những gì được bao hàm bởi thuật ngữ chung “các cấu trúc – structures”. Trong một cuộc họp đồng thuận đa ngành quốc tế từ năm 2021, một hội đồng chuyên gia gồm các bác sĩ Xquang, bác sĩ phẫu thuật, bác sĩ ung thư xạ trị, và bác sĩ bệnh học đã đề xuất rằng T4b nên bao gồm sự xâm lấn của các cấu trúc (structures) như đã đề cập trong hình trên.
5.1. T1-T2 – giới hạn ở thành ruột
Các khối u T1 và T2 giới hạn ở thành ruột và có tiên lượng tương đối tốt. Đặc điểm quan trọng để đảm bảo rằng một khối u vẫn giới hạn trong thành ruột (T1-2) là sự hiện diện của lớp đệm cơ còn nguyên vẹn (intact muscularis propria), có thể được nhận ra trên MRI như một đường tín hiệp thấp nguyên vẹn bao quanh trực tràng.
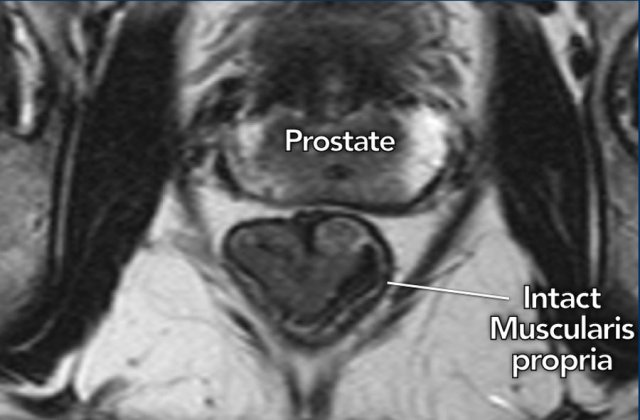
Hình 11. Một khối u cT1-2 ở trực tràng cho thấy lớp đệm cơ còn nguyên vẹn, có thể nhận biết rõ ràng là một đường nhỏ tín hiệu thấp bên ngoài thành trực tràng.
Cạm bẫy: phân biệt giai đoạn T1 với T2
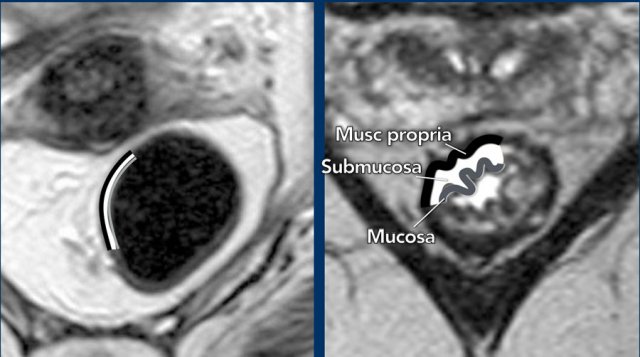 Hình 12. Về mặt giải phẫu, thành trực tràng bao gồm 3 lớp chính:
Hình 12. Về mặt giải phẫu, thành trực tràng bao gồm 3 lớp chính:
Lớp niêm mạc bên trong với tín hiệu trung gian trên hình ảnh T2W.
Lớp dưới niêm mạc giữa với tín hiệu cao trên hình ảnh T2W.
Lớp đệm cơ ngoài với tín hiệu thấp trên hình ảnh T2W.
Thông thường, 3 lớp riêng biệt này trên MRI chỉ có thể được nhận ra trong trường hợp phù nề dưới niêm mạc. Trong trường hợp không phù nề, thành trực tràng nhìn chung có hai lớp, nơi chúng ta có thể nhận ra lớp đệm nhưng không thể phân biệt niêm mạc với lớp dưới niêm mạc. Đây là lý do tại sao MRI nói chung không thể phân biệt các khối u T1 (phát triển vào lớp dưới niêm mạc) với các khối u T2 (phát triển vào lớp đệm cơ). Siêu âm nội soi chính xác hơn cho việc phân biệt này. Do đó, các khối u giới hạn trong thành trực tràng thường được xếp vào nhóm cT1-2 trên MRI.
5.2. T3 – xâm lấn vào lớp mỡ mạc treo trực tràng
Các khối u T3 phát triển qua lớp đệm cơ vào lớp mạc treo trực tràng xung quanh. Trên MRI, điều này có thể được nhận ra là sự gián đoạn của lớp đệm cơ tín hiệu thấp với sự mở rộng dạng hạt hoặc nốt của tín hiệu khối u vượt ra ngoài thành trực tràng vào lớp mỡ mạc treo trực tràng.
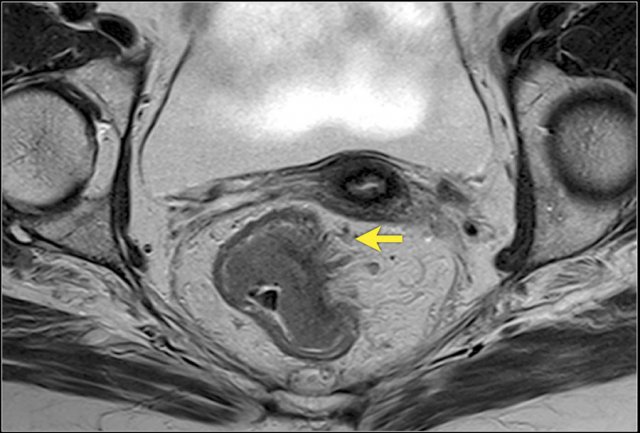
Hình 13. Một khối u trực tràng hình bán nguyệt với sự xâm lấn vào mạc treo trực tràng từ vị trí khoảng 1 đến 4 giờ. Nó không phát triển trong vòng 1mm của cân mạc treo trực tràng. Phân loại là ung thư trực tràng T3 MRF-.
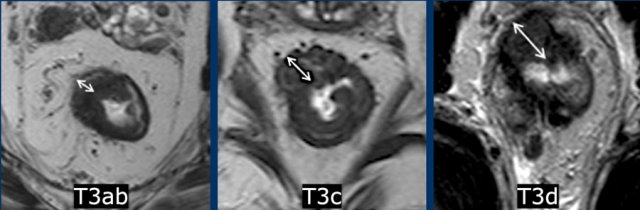 Hình 14. Phân loại giai đoạn T3 theo độ sâu xâm lấn (Subclassification of T3 stage according to invasion depth):
Hình 14. Phân loại giai đoạn T3 theo độ sâu xâm lấn (Subclassification of T3 stage according to invasion depth):
-Các khối u T3 nguy cơ thấp:
T3a: khối u kéo dài <1mm ra ngoài lớp đệm cơ
T3b: khối u kéo dài 1-5mm ra ngoài lớp đệm cơ
-Các khối u T3 nguy cơ cao:
T3c: khối u kéo dài 5-15mm ra ngoài lớp đệm cơ
T3d: khối u kéo dài >15mm ra ngoài lớp đệm cơ
T3 MRF+: bờ khối u cách MRF ≤ 1mm
Cạm bẫy: dải thâm nhiễm quanh trực tràng (perirectal stranding)
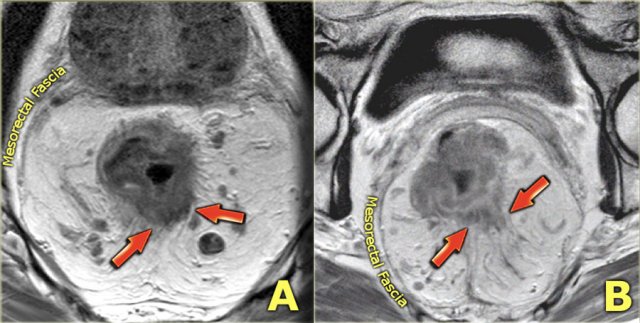 Hình 15. Có thể khó phân biệt sự xâm lấn thực sự của u quanh trực tràng ở các khối u T3 (case A) với vùng tạo mô sơ sợi dính (desmoplastic stranding) của các khối u T1-2 (case B), đây có thể là nguyên nhân tiềm ẩn cho việc phân độ quá mức.
Hình 15. Có thể khó phân biệt sự xâm lấn thực sự của u quanh trực tràng ở các khối u T3 (case A) với vùng tạo mô sơ sợi dính (desmoplastic stranding) của các khối u T1-2 (case B), đây có thể là nguyên nhân tiềm ẩn cho việc phân độ quá mức.
Ý nghĩa lâm sàng của việc phân biệt các khối u T2 với các khối u T3 đã được tranh luận trong nhiều hướng dẫn hiện hành – bao gồm cả các hướng dẫn của Hà Lan – phân loại các khối u T3 có phần mở rộng giới hạn trong mỡ mạc treo trực tràng (cT3ab) trong cùng một nhóm tiên lượng tốt như các khối u T2 để phân tầng điều trị. Tuy nhiên, trong một số hướng dẫn, bản thân các khối u T3 vẫn được coi là một yếu tố được sử dụng để xác định nhu cầu điều trị bổ trợ.
5.3. Liên quan đến cân mạc treo trực tràng (Mesorectal fascia involvement)
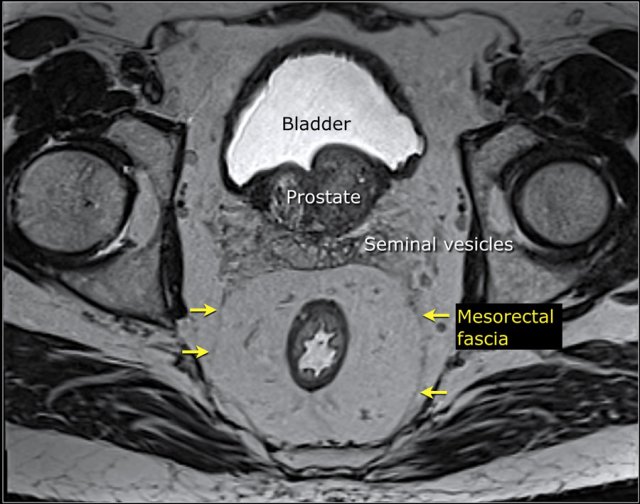
Hình 16. Cân mạc treo trực tràng (MRF – mesorectal fascia) là một cấu trúc dạng sợi mỏng (thin fibrous structure) bao quanh khoang mạc treo trực tràng và bao gồm mặt phẳng cắt bỏ được dự đoán trước trong phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng. Trên hình ảnh MRI T2W có thể nhận ra cân mạc treo trực tràng như một đường mỏng tín hiệu thấp bao quanh mạc treo trực tràng.
Khi một khối u xâm lấn trực tiếp vào cân mạc treo trực tràng hoặc ranh giới giữa khối u và cân mạc treo trực tràng ≤1mm, tức là có liên quan với cân mạc treo trực tràng. Trong những trường hợp này, phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng như thường quy sẽ gây ra nguy cơ tái phát cục bộ và điều trị bổ trợ sẽ được yêu cầu để làm giảm kích thước khối u để rút khối u ra khỏi cân mạc treo trực tràng nhằm đạt được biên độ cắt bỏ không có u. Khi mô tả sự tham gia của cân mạc treo trực tràng, bạn phải luôn mô tả vị trí của sự tham gia (ví dụ: “MRF+ tại vị trí …giờ” hoặc “MRF+ ở phía trước bên trái”)
Cạm bẫy: biên cắt bỏ theo chu vi (circumferential resection margin)
Một báo cáo chẩn đoán hình ảnh cho các khối u T3 phải gồm mô tả khoảng cách nhỏ nhất giữa khối u và cân mạc treo trực tràng, đôi khi được gọi cách khác trong các báo cáo X quang là ‘biên cắt bỏ theo chu vi – circumferential resection margin’.
Việc sử dụng biên cắt bỏ theo chu vi như một từ đồng nghĩa với MRF này không hoàn toàn chính xác vì biên cắt bỏ theo chu vi thực sự là do bác sĩ phẫu thuật tạo ra khi thực hiện phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng.
Lý tưởng nhất là phần này sẽ nằm dọc theo MRF, nhưng biên cắt bỏ theo chu vi có thể nhỏ hơn khi MRF bị vi phạm trong quá trình phẫu thuật hoặc rộng hơn khi mẫu cắt bỏ TME bao gồm thêm lớp mỡ bên ngoài MRF.
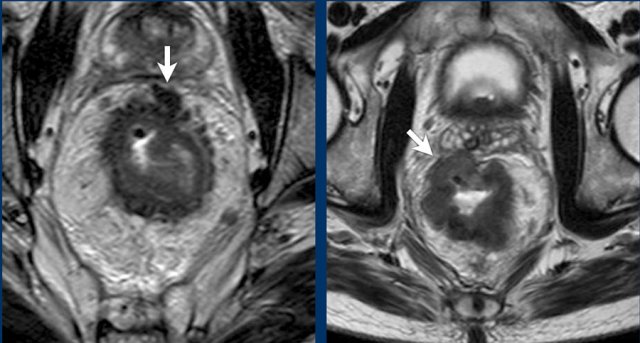
Hình 17. Hai ví dụ về các khối u T3 với sự xâm lấn cân mạc treo trực tràng. Trong trường hợp bên trái, khoảng cách giữa khối u và MRF nhỏ hơn 1mm ở 12 giờ. Trong trường hợp bên phải, có sự tham gia rộng hơn của MRF trong khoảng từ 10 đến 12 giờ.
5.4. Cân mạc treo trực tràng và phúc mạc (Mesorectal fascia versus Peritoneum)
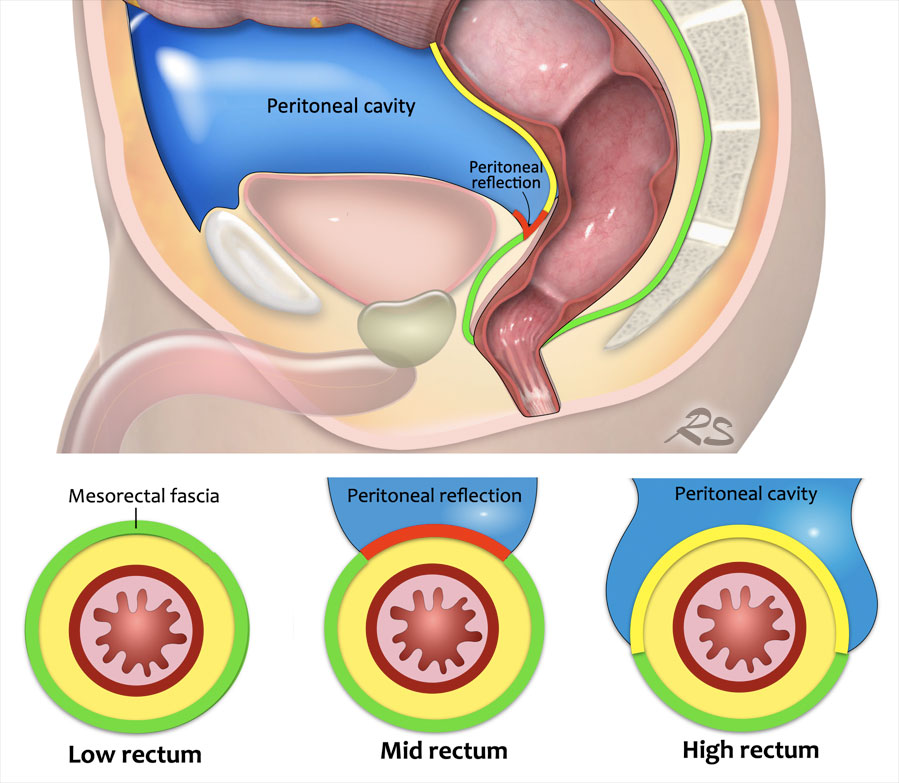 Hình 18. Trực tràng thấp được bao phủ hoàn toàn bởi mạc treo trực tràng (đường màu xanh lá cây).
Hình 18. Trực tràng thấp được bao phủ hoàn toàn bởi mạc treo trực tràng (đường màu xanh lá cây).
Trực tràng giữa, mạc treo trực tràng được bao phủ bởi cân mạc treo trực tràng ở mặt sau và mặt bên, nhưng ở phía trước nó được phúc mạc tạng bao phủ (đường màu đỏ cho thấy ngách phúc mạc).
Trực tràng cao, phúc mạc kéo dài từ phía trước sang phía bên (đường màu vàng) và cân mạc treo trực tràng chỉ bao phủ cho phần lưng của mạc treo trực tràng.
Sự phân biệt này rất quan trọng vì sự xâm lấn vào cân mạc treo trực tràng sẽ phân độ là T3 MRF+, trong khi sự phát triển vào phúc mạc tạng dẫn đến nguy cơ khối u di căn vào khoang phúc mạc và sẽ được phân độ là T4a.
5.5. T4a – Xâm lấn phúc mạc hoặc chỗ quặt ngược phúc mạc
Chỗ quặt ngược phúc mạc phía trước (the anterior peritoneal reflection) đánh dấu sự chuyển tiếp giữa phần không có phúc mạc (non-peritonealized portion) và phần có phúc mạc (peritonealized portion) của trực tràng.
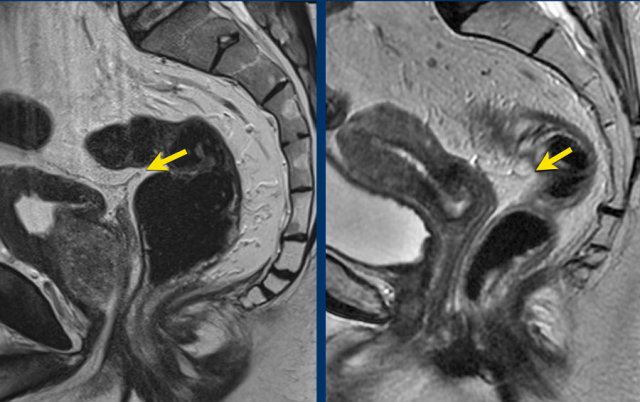
Hình 19. Trên hình ảnh T2W sagittal, chỗ quặt phúc mạc có thể được nhận ra như một đường mỏng hình chữ V tín hiệu thấp, đôi khi được gọi là ‘dấu hiệu mòng biển – seagull sign’. Ở nam giới, nó nằm ngay trên túi tinh. Ở nữ, nó nằm ở mức của túi cùng Douglas.
Cạm bẫy: Phân độ quá mức các khối u trực tràng cao
Ở những khối u trực tràng cao thường sẽ có một bờ gần giữa trực tràng và phúc mạc. Điều này không nhất thiết có nghĩa là nó khối u T4a. Các khối u chỉ nên được phân loại là cT4a nếu khối u mở rộng rõ ràng vào trong hoặc ra ngoài phúc mạc hoặc chỗ quặt phúc mạc.

Hình 20. Hình ảnh bên trái cho thấy một khối u có nằm gần phúc mạc và bàng quang (mũi tên trắng). Tuy nhiên, không có khối u mở rộng ra ngoài lớp đệm cơ phía trước, và phúc mạc do đó không bị xâm lấn. Hình ảnh bên phải cho thấy có sự xâm lấn rõ ràng vào phúc mạc (mũi tên vàng), nghĩa là khối u T4a.
Cạm bẫy: báo cáo xâm lấn MRF với xâm lấn phúc mạc
Lưu ý rằng trong các khối u phía trước, sự xâm lấn MRF chỉ có thể xảy ra ở các khối u nằm phía dưới chỗ quặt ngược phúc mạc. Các khối u phía trên chỗ quặt ngược phúc mạc sẽ xâm lấn vào phía trước phúc mạc (tức là khối u T4a) đôi khi được báo cáo nhầm là khối u MRF+ và điều này là không chính xác.
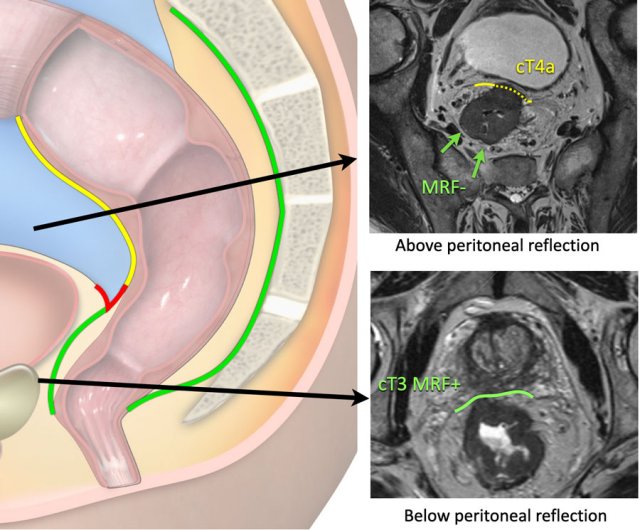 Hình 21. cT4a MRF-: Hình ảnh trên cho thấy một khối u cT4a ở trực tràng cao nằm trên mức quặt ngược phúc mạc. Có sự liên quan của phúc mạc (đường màu vàng), không phải của mạc treo trực tràng. cT3 MRF+: Hình ảnh bên dưới cho thấy một khối u cT3 ở trực tràng thấp nằm phía dưới mức quặt ngược phúc mạc. Có sự tham gia của mạc treo trực tràng ở phía trước (đường màu xanh lá cây), không phải của phúc mạc.
Hình 21. cT4a MRF-: Hình ảnh trên cho thấy một khối u cT4a ở trực tràng cao nằm trên mức quặt ngược phúc mạc. Có sự liên quan của phúc mạc (đường màu vàng), không phải của mạc treo trực tràng. cT3 MRF+: Hình ảnh bên dưới cho thấy một khối u cT3 ở trực tràng thấp nằm phía dưới mức quặt ngược phúc mạc. Có sự tham gia của mạc treo trực tràng ở phía trước (đường màu xanh lá cây), không phải của phúc mạc.
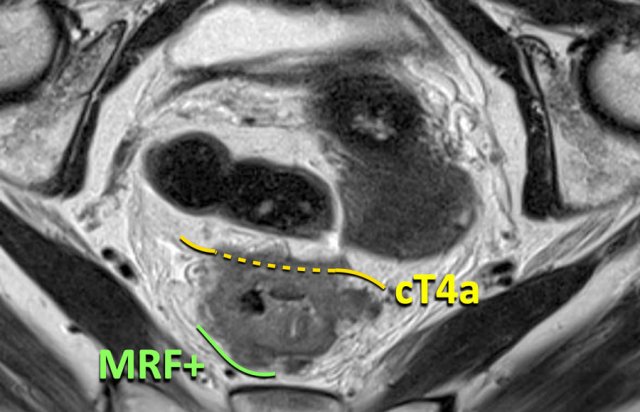 Hình 22. cT4a MRF+: Cũng có thể có sự kết hợp giữa liên quan phúc mạc và mạc treo trực tràng, như trong trường hợp này. Đây là một khối u ở trực tràng cao với sự liên quan của phúc mạc ở phía trước và mạc treo trực tràng ở phía sau.
Hình 22. cT4a MRF+: Cũng có thể có sự kết hợp giữa liên quan phúc mạc và mạc treo trực tràng, như trong trường hợp này. Đây là một khối u ở trực tràng cao với sự liên quan của phúc mạc ở phía trước và mạc treo trực tràng ở phía sau.
5.6. T4b – Xâm lấn các cơ quan hoặc cấu trúc xung quanh

Hình 23. Các khối u T4b xâm lấn các cơ quan hoặc cấu trúc khác nằm ngoài mạc treo trực tràng. Hội đồng đồng thuận năm 2021 đã đề xuất rằng giai đoạn T4b nên bao gồm việc mô tả xâm lấn các cấu trúc như đã đề cập trong hình.
Mặc dù đây là một chủ đề tranh luận, nhưng hội đồng đồng thuận đã đề xuất rằng sự xâm lấn T4b cũng nên bao gồm sự xâm lấn của bất kỳ lớp mỡ nào nằm trong một khoang giải phẫu khác bên ngoài khoang mạc treo trực tràng (tức là ngoài MRF), chẳng hạn như khoang bịt (obturator space), khoang quanh xương chậu (parailiac space) hoặc khoang ụ ngồi – trực tràng (ischiorectal space).
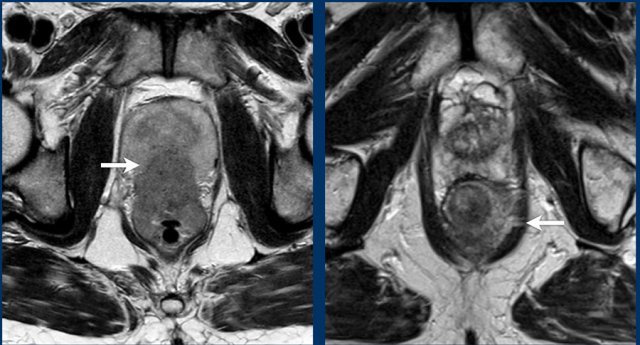
Hình 24. Ví dụ về khối u T4b với sự xâm lấn tuyến tiền liệt tương ứng (bên trái) và xâm lấn của cơ nâng hậu môn (bên phải).
Ghi chú:
Xâm lấn cơ vân (striated muscles) được coi là giai đoạn T4b, bao gồm xâm lấn cơ thắt ngoài hậu môn (external anal sphincter), cơ mu trực tràng (puborectalis) và cơ nâng hậu môn (levator ani muscles).
 Hình 25. Đây là một ví dụ về khối u cT4b phát triển vượt ra ngoài khoang mạc treo trực tràng vào lớp mỡ khoang bịt.
Hình 25. Đây là một ví dụ về khối u cT4b phát triển vượt ra ngoài khoang mạc treo trực tràng vào lớp mỡ khoang bịt.
5.7. Nhận ra giai đoạn xâm lấn T4b
Sự xâm lấn của khối u được định nghĩa là sự liên tục của tín hiệu khối u kéo dài sang cơ quan hoặc cấu trúc lân cận, thường đi kèm với mất lớp mỡ xen kẽ.
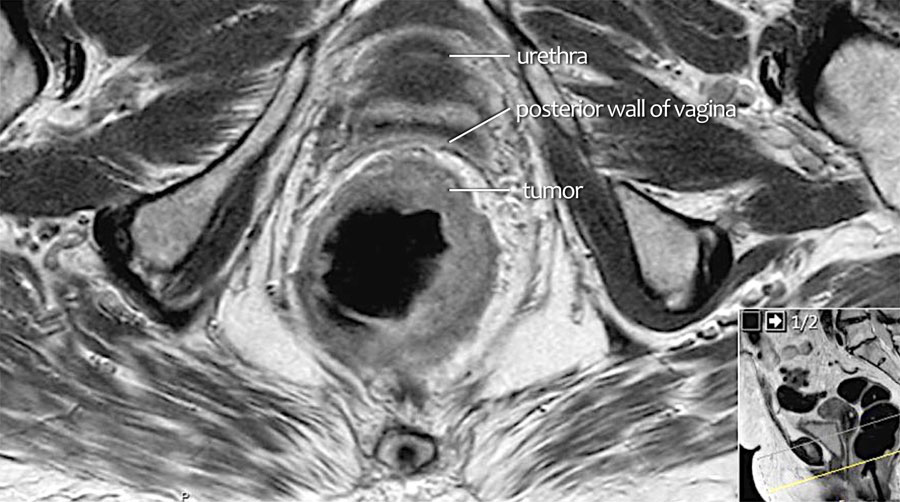
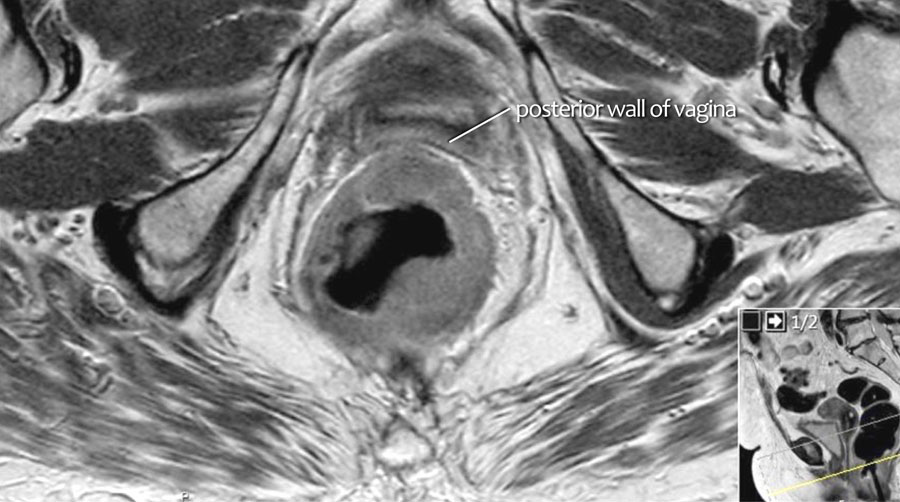
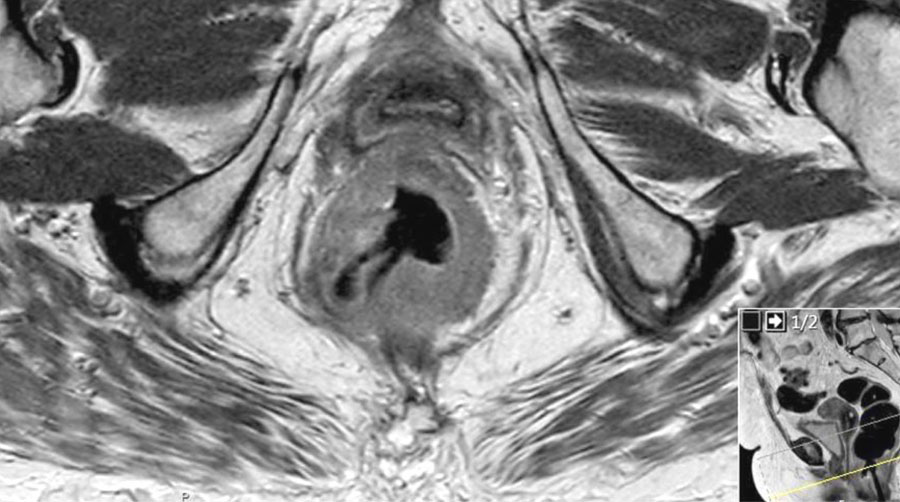
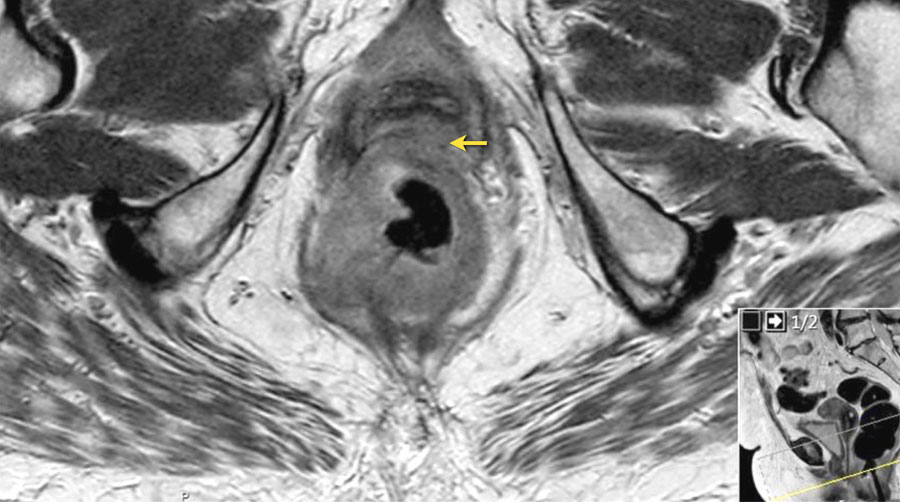
 Hình 26. Các hình ảnh cho thấy tín hiệu trung gian của khối u mở rộng vào thành sau của âm đạo (các mũi tên).
Hình 26. Các hình ảnh cho thấy tín hiệu trung gian của khối u mở rộng vào thành sau của âm đạo (các mũi tên).
5.8. EMVI – Xâm lấn mạch máu ngoài thành (Extramural vascular invasion)
Xâm lấn mạch máu ngoài thành là một yếu tố nguy cơ cho bệnh tái phát, di căn, và suy giảm khả năng sống sót toàn bộ.
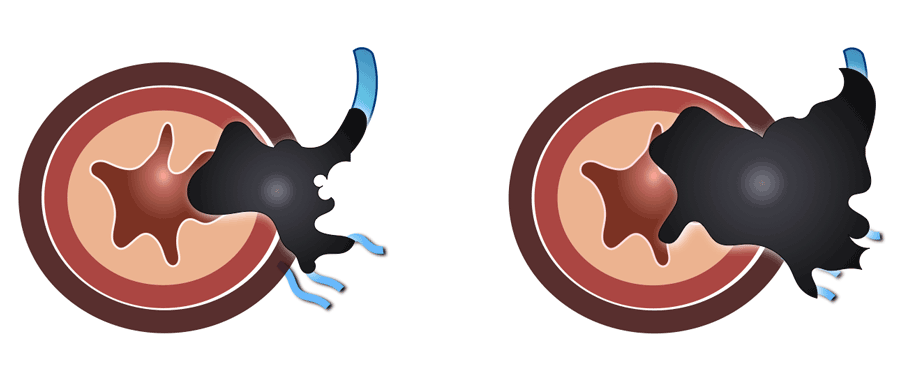
Hình 27. Xâm lấn mạch máu ngoài thành được nghi ngờ nếu thấy tín hiệu khối u kéo dài vào cấu trúc mạch máu gần khối u, khi mạch máu bị khối u làm mở rộng hoặc nếu khối u thâm nhiễm vào ranh giới của mạch máu (hình minh họa).
 Hình 28. Ví dụ về khối u xâm lấn mạch máu ngoài thành với tín hiệu khối u mở rộng vào cấu trúc mạch lân cận, mở rộng và phá vỡ đường viền mạch (expanding and disrupting the vessel contour).
Hình 28. Ví dụ về khối u xâm lấn mạch máu ngoài thành với tín hiệu khối u mở rộng vào cấu trúc mạch lân cận, mở rộng và phá vỡ đường viền mạch (expanding and disrupting the vessel contour).
Cạm bẫy: Làm thế nào để báo cáo sự liên quan của MRF bởi các hạch, lắng đọng mô u hoặc xâm lấn mạch máu ngoài thành? (How to report MRF involvement by nodes, tumor deposits or EMVI?)
Trong các hướng dẫn hiện hành, người ta không mô tả rõ ràng cách báo cáo sự tham gia của MRF bởi các cấu trúc mang khối u (tumor-bearing structures) khác với khối u nguyên phát (primary tumor).
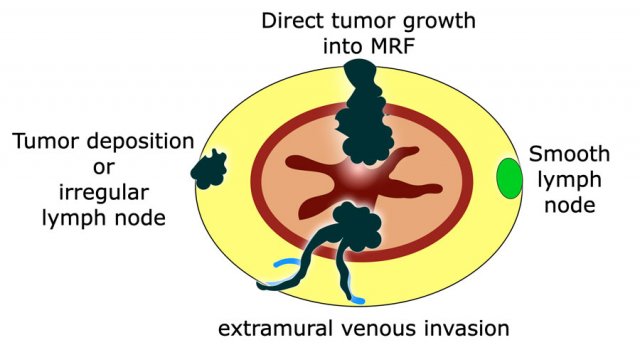 Hình 29. Hội đồng chuyên gia đa ngành vào năm 2021 đã đề xuất rằng MRF nên được báo cáo là liên quan nếu có biên độ ≤1mm từ khối u nguyên phát, xâm lấn tĩnh mạch ngoài thành (extramural venous invasion) hoặc từ lắng đọng mô u không đều (from irregularly enlarged tumor deposits) hoặc từ các hạch bạch huyết không đều (from irregular lymph nodes).
Hình 29. Hội đồng chuyên gia đa ngành vào năm 2021 đã đề xuất rằng MRF nên được báo cáo là liên quan nếu có biên độ ≤1mm từ khối u nguyên phát, xâm lấn tĩnh mạch ngoài thành (extramural venous invasion) hoặc từ lắng đọng mô u không đều (from irregularly enlarged tumor deposits) hoặc từ các hạch bạch huyết không đều (from irregular lymph nodes).
Các hạch bạch huyết mở rộng với bờ nhẵn và một vỏ bao rõ ràng còn nguyên vẹn tiếp xúc với MRF có tiềm năng ác tính với nguy cơ rất thấp dẫn đến liên quan đến bờ khi xét nghiệm mô bệnh học và do đó không nên được coi là MRF+ để tránh điều trị quá mức.
5.9. Liên quan cơ vòng hậu môn và sàn chậu
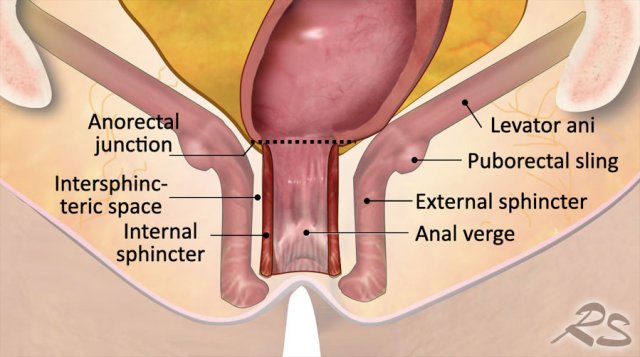 Hình 30. Cơ vòng hậu môn (anal sphincter, còn gọi là cơ thắt hậu môn) bao gồm ba lớp:
Hình 30. Cơ vòng hậu môn (anal sphincter, còn gọi là cơ thắt hậu môn) bao gồm ba lớp:
Cơ thắt trong: sự liên tục của cơ trơn trực tràng.
Khoang giữa cơ thắt: khoang giữa cơ thắt trong và ngoài
Cơ thắt ngoài: là cơ vân tự chủ. Ở phía trên, cơ thắt ngoài liên tục với cơ mu trực tràng và cơ nâng hậu môn.
Cùng với cơ ức chậu cụt (iliococcygeus muscle) và cơ mu cụt (pubococcygeus muscle), cơ mu trực tràng (puborectalis muscle) và cơ nâng hậu môn (levator ani muscle) tạo thành sàn chậu (pelvic floor). Trong ung thư trực tràng thấp, báo cáo MRI nên mô tả mối quan hệ của khối u với cơ thắt hậu môn và sàn chậu để hướng dẫn lập kế hoạch phẫu thuật và xạ trị. Điều này phải bao gồm mô tả về các lớp nào của cơ thắt hậu môn và / hoặc sàn chậu có liên quan; và liệu sự xâm lấn có kéo dài vào phần trên, giữa hoặc dưới của ống hậu môn hay không.
Cạm bẫy về cơ nâng hậu môn và TNM
Hệ thống phân giai đoạn TNM không xác định rõ ràng mức độ xâm lấn của các lớp khác nhau của cơ thắt hậu môn và sàn chậu nên được tính đến như thế nào.
 Hình 31. Trong cuộc họp đồng thuận chuyên gia năm 2021, nó đã được đề xuất rằng: Xác định giai đoạn cT chủ yếu dựa trên mức độ xâm lấn của khối u ở mức trực tràng. Loại trừ sự liên quan của cơ thắt trong và khoang gian cơ thắt để phân loại giai đoạn T. Sự liên quan của cơ thắt ngoài, cơ mu trực tràng hoặc cơ nâng hậu môn (skeletal muscle invasion = xâm lấn cơ vân = xâm lấn cơ xương) được phân loại là khối u cT4b.
Hình 31. Trong cuộc họp đồng thuận chuyên gia năm 2021, nó đã được đề xuất rằng: Xác định giai đoạn cT chủ yếu dựa trên mức độ xâm lấn của khối u ở mức trực tràng. Loại trừ sự liên quan của cơ thắt trong và khoang gian cơ thắt để phân loại giai đoạn T. Sự liên quan của cơ thắt ngoài, cơ mu trực tràng hoặc cơ nâng hậu môn (skeletal muscle invasion = xâm lấn cơ vân = xâm lấn cơ xương) được phân loại là khối u cT4b.
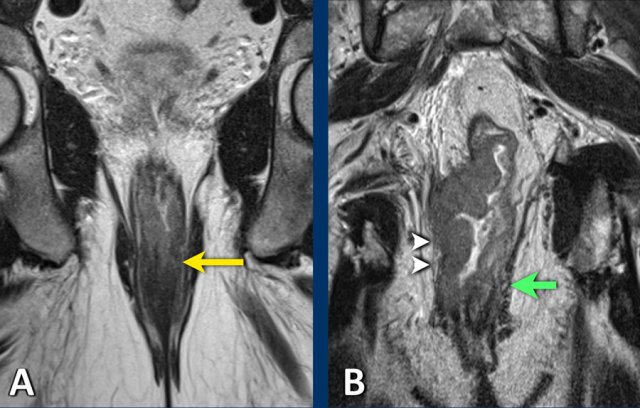
Hình 32. Hình A cho thấy một ví dụ về một khối u trực tràng thấp cT1-2 xâm lấn cơ thắt trong bên trái (mũi tên). Hãy nhớ rằng sự xâm lấn của cơ thắt trong không ảnh hưởng đến giai đoạn cT, nhưng cần được đề cập rõ ràng trong báo cáo MRI để giúp hướng dẫn lập kế hoạch phẫu thuật. Hình B là một ví dụ về một khối u trực tràng thấp xâm lấn vào cơ thắt trong và ngoài bên phải (các đầu mũi tên). Ngoài ra còn có sự tham gia của các cơ mu trực tràng và cơ nâng hậu môn. Hãy nhớ rằng sự xâm lấn của cơ thắt ngoài, cơ mu trực tràng và cơ nâng hâu môn tương đương với sự xâm lấn của cơ vân và nên được phân loại là khối u cT4b. Lưu ý sự xuất hiện bình thường của cơ thắt ngoài và cơ sàn chậu ở bên trái (mũi tên xanh).
6. Giai đoạn N
6.1. Bản đồ hạch
Thuật ngữ được sử dụng để mô tả các trạm hạch bạch huyết khác nhau trong ung thư trực tràng có thể gây nhầm lẫn.
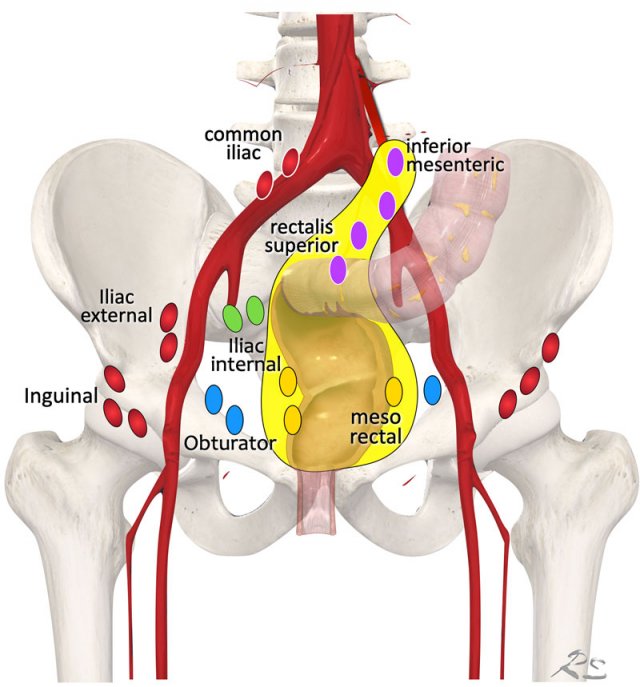
Hình 33. Dẫn lưu hạch vùng. Các hạch bạch huyết có màu đỏ là tất cả các hạch không phải hạch vùng (được xếp vào giai đoạn M). Trong phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng chỉ có các hạch mạc treo trực tràng và trong các khối u trực tràng cao cũng cắt bỏ các hạch mạc treo trực tràng trên và dưới.
Các hạch vùng (regional lymph nodes), bao gồm tất cả các hạch là một phần của giai đoạn N:
-Các hạch bạch huyết mạc treo trực tràng (màu vàng).
-Các hạch ở mạc treo đại tràng sigma, dọc theo mạc treo tràng dưới trước xương cùng và các mạch máu trực tràng trên (màu tím)
-Các hạch trong khoang bịt (màu xanh lam)
-Các hạch trong khoang quanh xương chậu trong (màu xanh lá cây).
Lưu ý rằng trong tiêu chuẩn phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng chỉ cắt bỏ các hạch ở mạc treo trực tràng và trong các khối u trực tràng cao cũng có các hạch mạc treo trực tràng trên và dưới (vùng màu vàng). Điều này có nghĩa là các hạch bạch huyết khu vực khác, nằm bên ngoài mạc treo trực tràng như hạch vùng bịt và chậu trong không được cắt bỏ thường quy.
Các hạch bạch huyết không phải hạch vùng (tất cả đều có màu đỏ), bao gồm tất cả các hạch – khi có liên quan – được coi là di căn hạch xa và do đó là một phần của giai đoạn M:
-Các hạch chậu ngoài
-Các hạch chậu chung
-Các hạch bẹn
Ghi chú: Một ngoại lệ đối với quy tắc này, AJCC TNM (xuất bản lần thứ 8) coi các hạch bẹn là các hạch khu vực trong trường hợp các khối u trực tràng thấp kéo dài đến ống hậu môn xa, dưới mức của đường lược (dentate line).
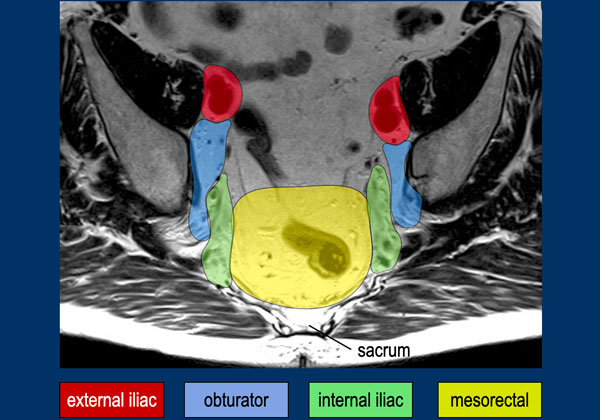 Hình 34. Hình ảnh MRI cho thấy các ngăn chứa hạch bạch huyết mạc treo trực tràng, chậu trong, bịt, chậu ngoài. Hãy nhớ rằng các hạch chậu ngoài không phải là hạch vùng và nếu dương tính, chúng được coi là bệnh di căn. Khoang bịt và chậu trong được phân chia bởi đường viền bên của thân chính của các mạch chậu trong. Đường viền sau của khoang chậu ngoài được xác định bởi đường viền sau của các mạch chậu ngoài.
Hình 34. Hình ảnh MRI cho thấy các ngăn chứa hạch bạch huyết mạc treo trực tràng, chậu trong, bịt, chậu ngoài. Hãy nhớ rằng các hạch chậu ngoài không phải là hạch vùng và nếu dương tính, chúng được coi là bệnh di căn. Khoang bịt và chậu trong được phân chia bởi đường viền bên của thân chính của các mạch chậu trong. Đường viền sau của khoang chậu ngoài được xác định bởi đường viền sau của các mạch chậu ngoài.

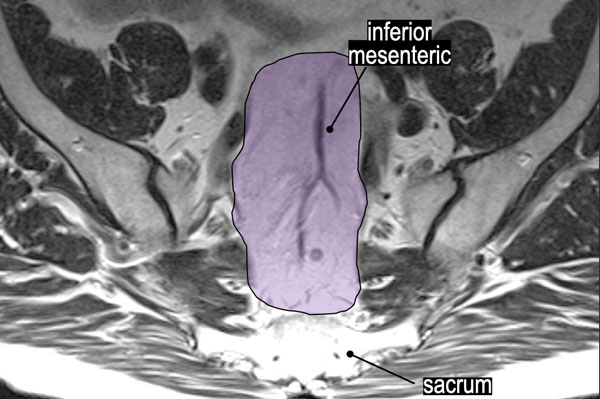 Hình 35. Trong vùng màu tím có các hạch mạc treo trực tràng trên và mạc treo tràng dưới. Các hạch này đôi khi được gọi là “hạch mạc treo trực tràng cao – high mesorectal nodes” và là một phần của các hạch vùng để phân giai đoạn N. Mức độ của hạch đáng ngờ cao nhất trong khu vực này nên được đề cập trong báo cáo, vì điều này sẽ ảnh hưởng đến trường xạ trị đã chọn.
Hình 35. Trong vùng màu tím có các hạch mạc treo trực tràng trên và mạc treo tràng dưới. Các hạch này đôi khi được gọi là “hạch mạc treo trực tràng cao – high mesorectal nodes” và là một phần của các hạch vùng để phân giai đoạn N. Mức độ của hạch đáng ngờ cao nhất trong khu vực này nên được đề cập trong báo cáo, vì điều này sẽ ảnh hưởng đến trường xạ trị đã chọn.
6.2. Các hạch mạc treo trực tràng
Giai đoạn N trong ung thư trực tràng chỉ dựa trên số lượng các hạch vùng nghi ngờ. Các hạch không vùng nghi ngờ được coi là hạch di căn. MRI giống như các phương thức hình ảnh khác có hiệu suất chẩn đoán tương đối thấp đối với các giai đoạn hạch bạch huyết. Liệu giai đoạn N được xác định bằng hình ảnh có nên được xem xét để phân tầng điều trị hay không vẫn là chủ đề tranh luận, mặc dù hầu hết các hướng dẫn hiện nay vẫn coi giai đoạn N dương tính trên hình ảnh là một dấu hiệu nguy cơ cao, cần được điều trị bổ trợ. Kết quả tốt nhất thu được khi áp dụng sự kết hợp giữa kích thước và hình thái hạch để mô tả các hạch bạch huyết ở mạc treo trực tràng.
Các hạch ≥9mm và các hạch có đặc điểm tín hiệu nhầy luôn được coi là đáng ngờ. Các hạch nhỏ hơn cần có thêm các đặc điểm đáng ngờ về hình thái (hình tròn, đường viền không rõ ràng, tín hiệu không đồng nhất) để được coi là cN+ như chi tiết trong hình.
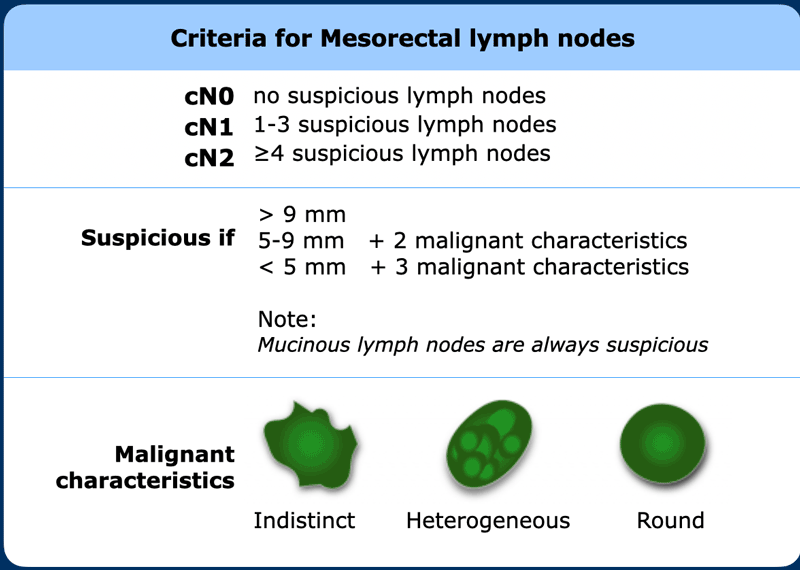 Hình 36. Tiêu chí của các hạch mạc treo trực tràng.
Hình 36. Tiêu chí của các hạch mạc treo trực tràng.
Ghi chú: Điều quan trọng là phải đề cập đến mức độ của các hạch nghi ngờ gần nhất, đặc biệt nếu có các hạch N+ cao hiện diện ở mạc treo trực tràng hoặc ở mạc treo đại tràng sigma đoạn xa, dọc theo các mạch trực tràng trên hoặc mạc treo tràng dưới, vì các hạch này có thể tác động đến trường xạ trị. Các tiêu chí về kích thước + hình thái giống nhau được áp dụng cho các hạch mạc treo trực tràng cao (high mesorectal) này.
6.3. Các hạch bên
Các hạch bên đôi khi được gọi là các hạch ngoài trực tràng (extramesorectal lymph nodes). Đây là những hạch nằm ở phía ngoài mạc treo trực tràng và không được cắt bỏ thường quy trong phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng tiêu chuẩn. Chúng cần được xem xét cẩn thận và được đề cập riêng trong báo cáo. Đặc biệt các khối u nằm dưới chỗ quặt phúc mạc có xu hướng lan vào các khoang chậu trong và khoang bịt. Nếu các hạch bệnh lý trong các ngăn này không được điều trị bổ sung bằng cách phẫu thuật bóc tách hạch bên hoặc xạ trị, chúng có nguy cơ tái phát cao hơn.
 Hình 37. Vào năm 2019, nhóm nghiên cứu hạch bên đã đề xuất ngưỡng kích thước (size cut-off) cắt bỏ nếu đường kính trục ngắn ≥7mm cho giai đoạn các hạch chậu trong và hạch bịt trên MRI và cũng cho thấy rằng – không giống như ở các hạch mạc treo trực tràng – các đặc điểm hình thái không nên tính vào.
Hình 37. Vào năm 2019, nhóm nghiên cứu hạch bên đã đề xuất ngưỡng kích thước (size cut-off) cắt bỏ nếu đường kính trục ngắn ≥7mm cho giai đoạn các hạch chậu trong và hạch bịt trên MRI và cũng cho thấy rằng – không giống như ở các hạch mạc treo trực tràng – các đặc điểm hình thái không nên tính vào.
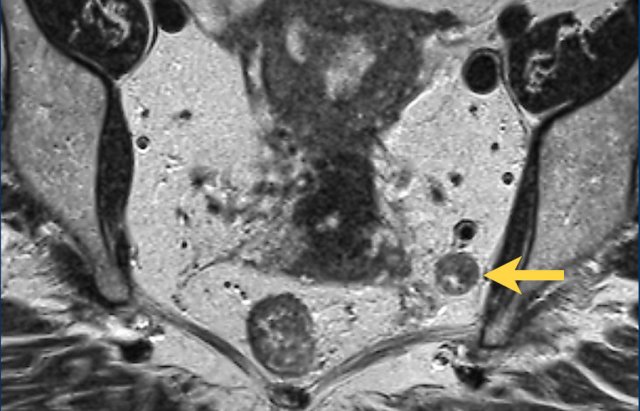 Hình 38. Ví dụ về một hạch bệnh lý có kích thước 9mm ở khoang bịt bên trái (mũi tên). Hạch này cần được chiếu xạ hoặc cắt bỏ riêng biệt để tránh tái phát.
Hình 38. Ví dụ về một hạch bệnh lý có kích thước 9mm ở khoang bịt bên trái (mũi tên). Hạch này cần được chiếu xạ hoặc cắt bỏ riêng biệt để tránh tái phát.
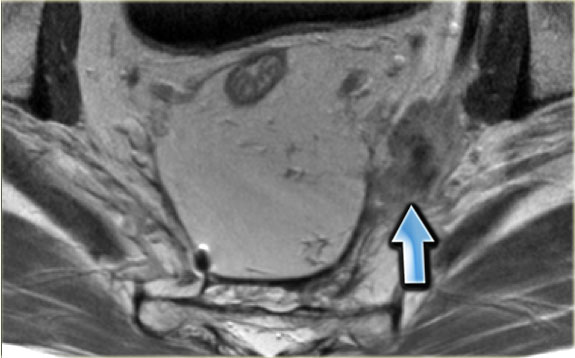 Hình 39. Hình ảnh T2W axial một bệnh nhân đã được điều trị phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng. Có sự tái phát cục bộ của ung thư trực tràng do một hạch bên dương tính không được điều trị.
Hình 39. Hình ảnh T2W axial một bệnh nhân đã được điều trị phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng. Có sự tái phát cục bộ của ung thư trực tràng do một hạch bên dương tính không được điều trị.
 Hình 40. Mặc dù không được sử dụng thường quy bởi tất cả phân độ trên hình ảnh học, ấn bản thứ 8 của TNM phân chia thêm giai đoạn N.
Hình 40. Mặc dù không được sử dụng thường quy bởi tất cả phân độ trên hình ảnh học, ấn bản thứ 8 của TNM phân chia thêm giai đoạn N.
Cạm bẫy: hạch so với lắng đọng mô u (nodes versus tumor deposits)
Các hạch bệnh lý và lắng đọng mô u có thể trông rất giống nhau trên hình ảnh và không có tiêu chí nào được chấp nhận rộng rãi để phân biệt hai loại này. Một số định nghĩa lắng đọng mô u là các nốt không đều hơn thường nằm trong hoặc dọc theo các mạch máu, trong khi các hạch bệnh lý vẫn có hình dạng tròn hoặc bầu dục quen thuộc và có vỏ điển hình của các hạch bạch huyết. Tuy nhiên, những định nghĩa này vẫn còn được xác nhận trên quy mô lớn. Cho đến lúc đó, hội đồng đồng thuận năm 2021 khuyên nên nhóm các hạch và lắng động mô u lại với nhau trong giai đoạn cN. Mô tả chung về kích thước và hình thái của các tổn thương đáng ngờ nên được đưa vào báo cáo.
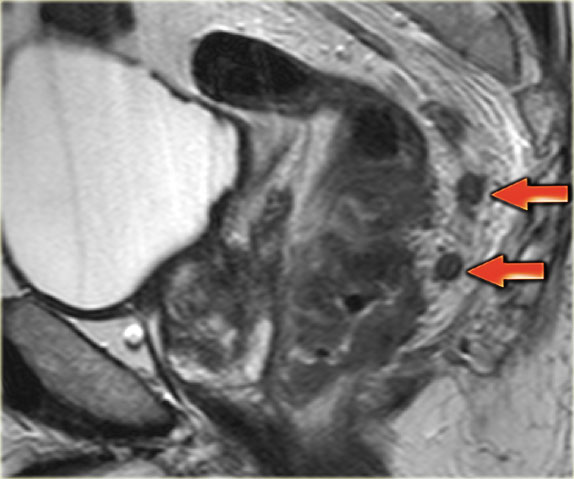
Hình 41. Hình ảnh T2W sagittal cho thấy ung thư trực tràng thấp với nhiều tổn thương dạng nốt không đều ở lớp mỡ mạc treo trực tràng ở mặt sau. Mặc dù người ta có thể tranh luận liệu những tổn thương này đại diện cho khối u hay hạch bệnh lý, nhưng chúng đều được coi là một phần của giai đoạn N, là cN2 ở bệnh nhân này. Kết hợp với giai đoạn T nâng cao (T3c MRF+), bệnh nhân này được phân loại là tiến triển tại chỗ và được hóa xạ trị bổ trợ cho khối u và hạch để giảm độ.
7. Giai đoạn M
 Hình 42. Giai đoạn M trong ung thư trực tràng dựa trên sự hiện diện của các di căn hạch không vùng đáng ngờ (suspicious non-regional lymph node metastases) và các di căn xa khác (other distant metastases). Lưu ý rằng các hạch bạch huyết ngoài vùng được coi là một “organ – cơ quan”.
Hình 42. Giai đoạn M trong ung thư trực tràng dựa trên sự hiện diện của các di căn hạch không vùng đáng ngờ (suspicious non-regional lymph node metastases) và các di căn xa khác (other distant metastases). Lưu ý rằng các hạch bạch huyết ngoài vùng được coi là một “organ – cơ quan”.
8. Đánh giá lại sau điều trị bổ trợ
8.1. Danh mục kiểm tra
Về cơ bản, một báo cáo đánh giá lại giai đoạn sử dụng các bộ mô tả giống như đối với phân loại đầu tiên. Ngoài việc phân loại yTNM, điều quan trọng là phải đưa ra ước tính tổng thể về mức độ đáp ứng và phân loại bệnh nhân là người đáp ứng kém, tốt, tiềm năng đáp ứng hoàn toàn để cung cấp thêm thông tin cho việc đưa ra quyết định lâm sàng. Trong hầu hết các trường hợp, báo cáo đánh giá lại giai đoạn chủ yếu đóng vai trò là một lộ trình cập nhật cho bác sĩ phẫu thuật. Trong một số trường hợp, việc đánh giá lại cũng được sử dụng để lựa chọn các ứng viên tiềm năng cho việc bảo tồn nội tạng.

Hình 43. Trong hình, các mục và tiêu chí chính dành riêng cho việc đánh giá lại giai đoạn được tóm tắt.
8.2. Đánh giá đáp ứng
Sau khi hóa xạ trị, các khối u trực tràng thường giảm kích thước và trải qua một sự chuyển dạng sợi, có thể quan sát thấy sự giảm rõ rệt tín hiệu của giường khối u trên hình ảnh T2W. Trong một số ít trường hợp (<5%), khối u hoàn toàn biến mất và thành trực tràng dường như bình thường xuất hiện trở lại trên MRI sau hóa xạ trị. Một báo cáo MRI đánh giá lại giai đoạn nên bắt đầu bằng mô tả chung về mức độ đáp ứng.
Mức độ đáp có thể được phân loại thành:
-Đáp ứng gần hoàn toàn hoặc có thể hoàn toàn khi có thành trực tràng bình thường hoặc chỉ xơ hóa.
-Đáp ứng tốt với xơ hóa chiếm ưu thế nhưng nghi ngờ khối u nhỏ còn sót lại trong vùng xơ hóa trên MRI T2W hoặc DWI.
-Đáp ứng kém với phần lớn là tàn tích khối u đặc.
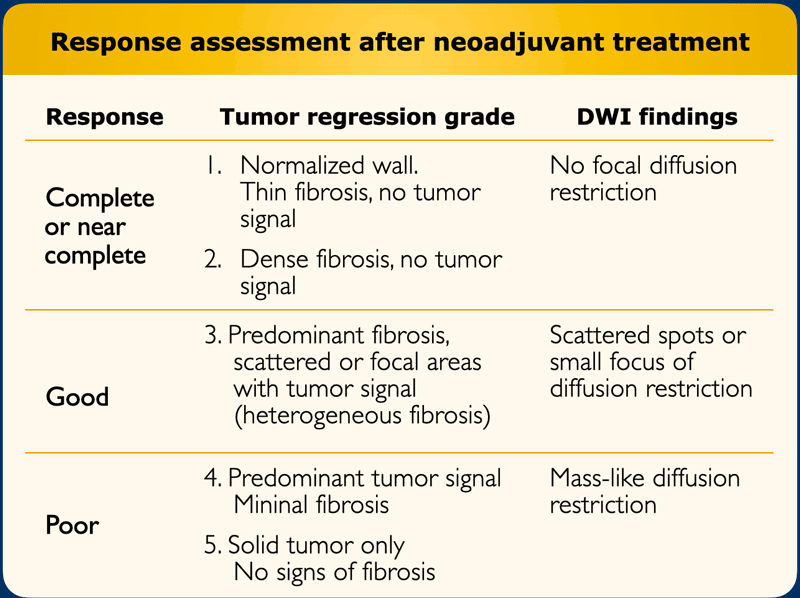 Hình 44. Phân độ thoái triển khối u (Tumor regression grade). MRI đã biết những khó khăn trong việc phân biệt giữa xơ hóa vẫn chứa các tế bào u và xơ hóa đơn thuần. Tuy nhiên, có một số mô hình nhất định có thể giúp ước tính nguy cơ đối với khối u tồn tại đáng kể trong xơ hóa. Phân độ thoái triển khối u trên MRI (the MR tumor regression grade) là sự thích ứng hình ảnh của các hệ thống phân độ thoái triển khối u tương tự được sử dụng trong mô bệnh học và có thể được sử dụng để đánh giá mức độ biến đổi sợi trên MRI T2W bằng thang điểm 5.
Hình 44. Phân độ thoái triển khối u (Tumor regression grade). MRI đã biết những khó khăn trong việc phân biệt giữa xơ hóa vẫn chứa các tế bào u và xơ hóa đơn thuần. Tuy nhiên, có một số mô hình nhất định có thể giúp ước tính nguy cơ đối với khối u tồn tại đáng kể trong xơ hóa. Phân độ thoái triển khối u trên MRI (the MR tumor regression grade) là sự thích ứng hình ảnh của các hệ thống phân độ thoái triển khối u tương tự được sử dụng trong mô bệnh học và có thể được sử dụng để đánh giá mức độ biến đổi sợi trên MRI T2W bằng thang điểm 5.
8.3. Hình ảnh khuếch tán
DWI làm nổi bật mô có mật độ tế bào cao, trong đó sự di chuyển ra ngoài tế bào của nước bị hạn chế. DWI đã được chứng minh là một công cụ hỗ trợ hữu ích cho T2W để chẩn đoán sự hiện diện của khối u tồn dư còn sót lại trong giường khối u đã thay đổi sợi sau khi hóa xạ trị. Trong trường hợp khối u còn sót lại, tín hiệu cao thường có thể được quan sát thấy ở rìa trong của vùng xơ hóa trên hình ảnh DWI với giá trị b cao, với tín hiệu thấp tương ứng trên bản đồ ADC.
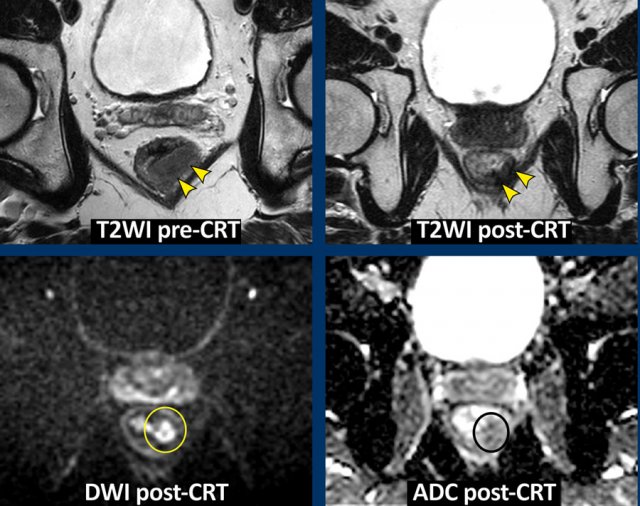 Hình 45. Hình ảnh T2W trước điều trị và sau hóa xạ trị với xơ hóa chiếm ưu thế với tín hiệu không đồng nhất (TRG 3). DWI tương ứng sau điều trị cho thấy một vùng khu trú của tín hiệu cao ở rìa trong của vùng xơ hóa tương ứng với tín hiệu thấp trên bản đồ ADC, cho thấy sự khuếch tán hạn chế. Đây được xác nhận là một khối u nhỏ còn sót lại (ypT2) tại trên mô bệnh học.
Hình 45. Hình ảnh T2W trước điều trị và sau hóa xạ trị với xơ hóa chiếm ưu thế với tín hiệu không đồng nhất (TRG 3). DWI tương ứng sau điều trị cho thấy một vùng khu trú của tín hiệu cao ở rìa trong của vùng xơ hóa tương ứng với tín hiệu thấp trên bản đồ ADC, cho thấy sự khuếch tán hạn chế. Đây được xác nhận là một khối u nhỏ còn sót lại (ypT2) tại trên mô bệnh học.
Cạm bẫy: phân giai đoạn trong trường hợp xơ hóa (Pitfall: staging in case of fibrosis)
Thật không may, độ chính xác tổng thể của MRI để đánh giá giai đoạn yT, yMRF, yEMVI và xâm lấn cơ vòng sau hóa xạ trị kém hơn so với phân độ trước điều trị do những khó khăn của MRI để đánh giá sự hiện diện và phạm vi của khối u quan trọng trong giường khối u đã bi thay đổi sợi.
Đánh giá sự liên quan của MRF sau hóa xạ trị
Khi một mặt phẳng mỡ xuất hiện trở lại giữa giường khối u và MRF sau hóa xạ trị, nguy cơ liên quan đến MRF là rất nhỏ.
Khi vẫn còn sự xâm nhập lan tỏa của MRF bởi tín hiệu trung gian khối u sau hóa xạ trị, thì nguy cơ khối u xâm lấn ở mô bệnh học là cao (khoảng 90%). Những trường hợp khó nhất là những trường hợp MRF thâm nhiễm sợi lan tỏa. Trong những trường hợp này, nguy cơ dương tính với MRF ở mô bệnh học là khoảng 50%.
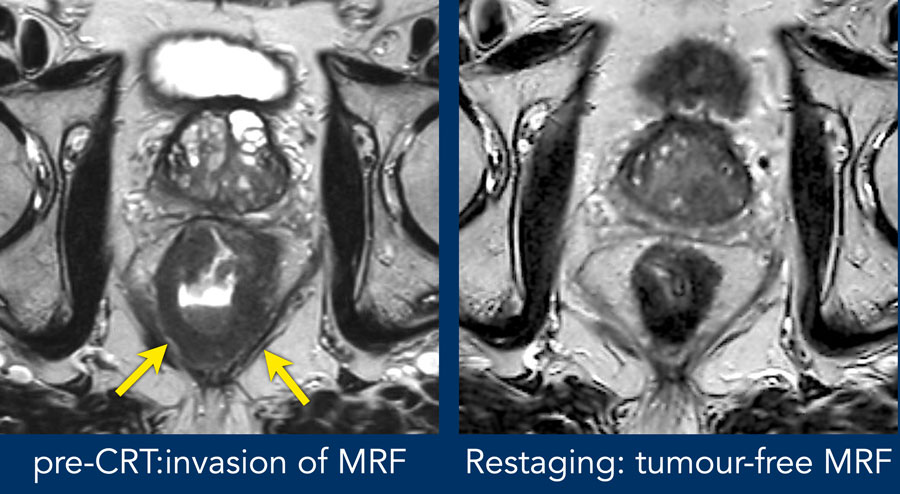 Hình 46. Trước điều trị có sự xâm nhập rộng rãi của MRF từ vị trí 4-8 giờ (mũi tên). Sau khi hóa xạ trị, khối u đã trải qua một quá trình biến đổi sợi và đã rút khỏi MRF. Một lớp mỡ đã xuất hiện chỉ với một số sợi nhỏ mắc kéo về phía MRF. Đây là những dấu hiệu cho thấy MRF không có khối u khi đánh giá lại giai đoạn (yMRF-).
Hình 46. Trước điều trị có sự xâm nhập rộng rãi của MRF từ vị trí 4-8 giờ (mũi tên). Sau khi hóa xạ trị, khối u đã trải qua một quá trình biến đổi sợi và đã rút khỏi MRF. Một lớp mỡ đã xuất hiện chỉ với một số sợi nhỏ mắc kéo về phía MRF. Đây là những dấu hiệu cho thấy MRF không có khối u khi đánh giá lại giai đoạn (yMRF-).
Giai đoạn yN
Hiệu suất chẩn đoán của MRI để đánh giá lại các hạch bạch huyết sau hóa xạ trị tốt hơn so với giai đoạn trước hóa xạ trị. Sau hóa xạ trị, phần lớn các hạch giảm kích thước hoặc biến mất hoàn toàn trên MRI. Các hạch vẫn nhìn thấy rõ ràng sau hóa xạ trị vẫn có nguy cơ.
Mặc dù giới hạn kích thước tối ưu vẫn còn là một chủ đề tranh luận, ngưỡng giới hạn ≥5mm (đường kính trục ngắn) đã được đề xuất để chẩn đoán các hạch yN+ sau hóa xạ trị. Đối với các hạch bên, tổ hợp nghiên cứu hạch bên đã đề xuất ngưỡng cut-off >4mm (hạch chậu trong) và >6mm (hạch bịt), nhưng các tiêu chí này cho đến nay được coi là sơ bộ và vẫn còn được xác nhận.
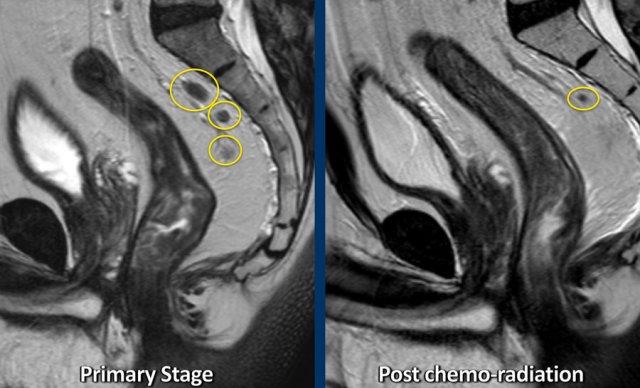
Hình 47. Ví dụ về một bệnh nhân có một số hạch cN+ to ra bất thường ở giai đoạn trước hóa xạ trị. Sau khi hóa xạ trị, hầu hết các hạch đã biến mất và chỉ còn lại một hạch nhỏ <5mm, là dấu hiệu của giai đoạn ycN0.
Các hạch bạch huyết giống như các mô bạch huyết khác bao gồm lách có cấu trúc tế bào dày đặc dẫn đến sự khuếch tán bị hạn chế và tín hiệu cao trên DWI. Kết quả là, DWI có thể hữu ích trong việc phát hiện các hạch bạch huyết nhưng ít phù hợp hơn để xác định đặc điểm của hạch bạch huyết vì cả hạch bạch huyết lành tính và di căn sẽ cho tín hiệu cao.
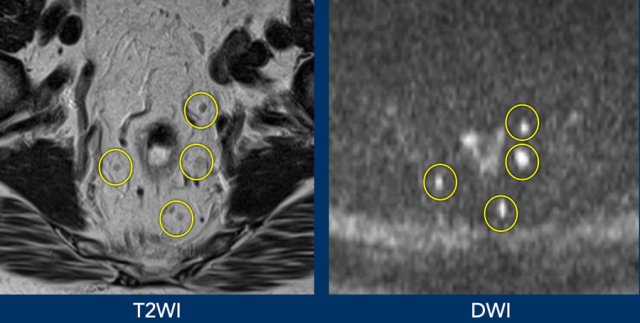
Hình 48. Hình ảnh hạch bạch huyết được quan sát tốt hơn trên DWI so với T2W tương ứng.
8.4. Cạm bẫy DWI
Hiệu ứng T2 quá sáng (T2 shine through)
Hình ảnh DWI vốn dĩ là T2W. Hiệu ứng T2 quá sáng đề cập đến sự hiện diện của tín hiệu cao trên DWI không phải do khuếch tán hạn chế, mà do thời gian T2 dài (ví dụ, trong chất lỏng). Trong DWI trực tràng, điều này có thể xảy ra trong trường hợp có một lượng nhỏ chất lỏng trong lòng trực tràng, có thể giống khối u ở thành trực tràng lân cận. Để phân biệt giữa sự ảnh giả do hiệu ứng này và khối u thì cần phải tham khảo bản đồ ADC (nếu DWI sáng và ADC sáng thì đó là chất lỏng, nếu DWI sáng và ADC tối thì đó là mô u).
Hiệu ứng T2 quá tối (T2 dark through)
Còn được gọi là T2 black out, đề cập đến tín hiệu thấp rõ rệt được quan sát trên bản đồ ADC ở những khu vực xơ hóa dày đặc mà không có khối u. Điều này xảy ra ở các mô có thời gian giãn T2 rất ngắn (chẳng hạn như xơ hóa giàu collagen, tổn thương vôi hóa, và vỏ xương) và sẽ dẫn đến tín hiệu thấp hoàn toàn trên bản đồ ADC, cũng như trên các chuỗi xung khác bao gồm DWI, T2W và T1W. Hiệu ứng T2 quá tối không nên nhầm với hạn chế khuếch tán nghi ngờ khối u.
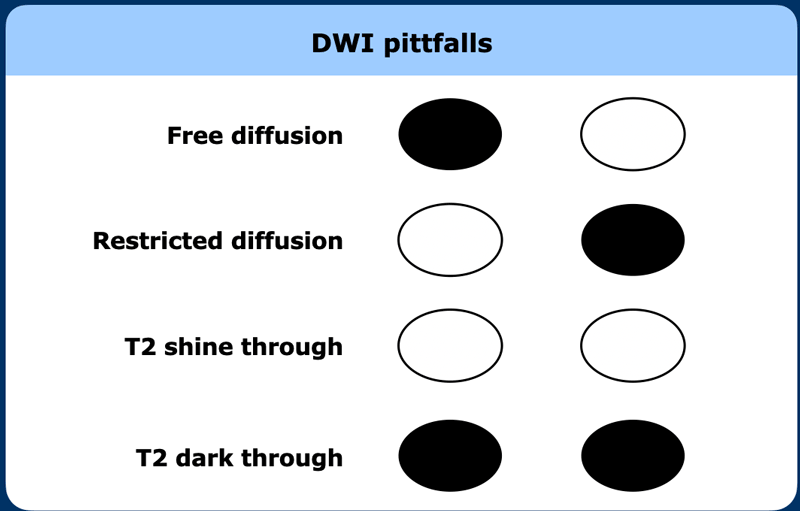
Hình 49. Mô tả tín hiệu trên DWI và ADC
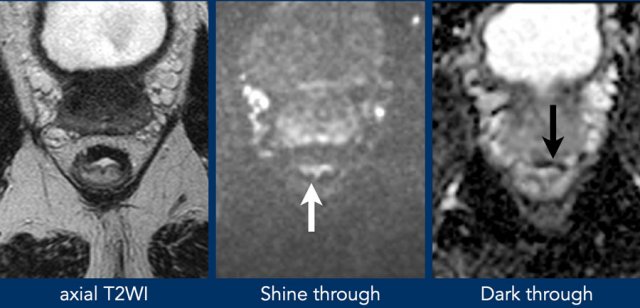 Hình 50. (A, B) Ví dụ về hiệu ứng T2 quá sáng, hình ảnh T2W và DWI đều có tín hiệu cao do chất lỏng trong lòng trực tràng. (C) Ví dụ về hiệu ứng T2 quá tối, bản đồ ADC cho thấy tín hiệu rất thấp trong thành trực tràng do bị thay đổi sợi. Không có tín hiệu cao tương ứng trong thành trên DWI, nghĩa là thực tế không có hạn chế khuếch tán.
Hình 50. (A, B) Ví dụ về hiệu ứng T2 quá sáng, hình ảnh T2W và DWI đều có tín hiệu cao do chất lỏng trong lòng trực tràng. (C) Ví dụ về hiệu ứng T2 quá tối, bản đồ ADC cho thấy tín hiệu rất thấp trong thành trực tràng do bị thay đổi sợi. Không có tín hiệu cao tương ứng trong thành trên DWI, nghĩa là thực tế không có hạn chế khuếch tán.
Ảnh giả nhạy từ (susceptibility artefacts)
Hình ảnh DWI trong ổ bụng thường được thực hiện bằng cách sử dụng hình ảnh điểm vang đồng phẳng (EPI), cho phép thu nhận hình ảnh nhanh chóng do đó giảm thiểu nguy cơ ảnh giả do chuyển động. Nhược điểm chính của EPI-DWI là nó rất dễ bị các hiệu ứng nhạy từ, tức là biến dạng hoặc chồng chất giả tạo của tín hiệu MRI do không đồng nhất từ trường cục bộ, đặc biệt là ở nếu máy MRI có từ trường cao hơn. Trong DWI trực tràng, những hiệu ứng nhạy cảm này chủ yếu xảy ra ở phần tiếp giáp giữa mô mềm trong thành trực tràng hoặc khối u và khí trong lòng. Trong khi các xảo ảnh lớn sẽ dễ dàng được nhận ra là ảnh giả, những xảo ảnh nhỏ hơn qua thành trực tràng có thể bị hiểu nhầm là tín hiệu khối u. Có thể tránh được hiện tượng này trong DWI trực tràng bằng cách giảm lượng khí trong lòng trực tràng hoặc bằng cách sử dụng các phương pháp thu nhận DWI thay thế, chẳng hạn như kỹ thuật spin echo, ít bị các ảnh giả nhạy từ hơn.
 Hình 51. Đây là một bệnh nhân có khối u ở thành trước bên trực tràng bên phải. Sau hóa xạ trị, có thể nhìn thấy xơ hóa tại vị trí của giường khối u trước đây từ 9-12 giờ. Tín hiệu cao trên DWI nằm ở phía bên cạnh, bên ngoài giường khối u và tương ứng với các hiện tượng nhạy từ do khí trong lòng trực tràng gây ra. Không nên nhầm những ảnh giả này với tín hiệu cao nghi ngờ khối u.
Hình 51. Đây là một bệnh nhân có khối u ở thành trước bên trực tràng bên phải. Sau hóa xạ trị, có thể nhìn thấy xơ hóa tại vị trí của giường khối u trước đây từ 9-12 giờ. Tín hiệu cao trên DWI nằm ở phía bên cạnh, bên ngoài giường khối u và tương ứng với các hiện tượng nhạy từ do khí trong lòng trực tràng gây ra. Không nên nhầm những ảnh giả này với tín hiệu cao nghi ngờ khối u.
9. MRI protocol
9.1. Phần cứng
MRI ung thư trực tràng có thể được thực hiện ở máy 1.5T hoặc 3.0T, sử dụng các coils bề mặt. Việc sử dụng một coil nội trực tràng không được khuyến nghị thường quy.
9.2. Chuẩn bị cho bệnh nhân
Việc chuẩn bị cho bệnh nhân là không bắt buộc. Việc sử dụng thuốc giảm co thắt có thể được xem xét để làm giảm nhu động ruột (đặc biệt ở các khối u trực tràng cao dễ bị các ảnh giả hơn). Sử dụng chất làm đầy nội lòng trực tràng không được khuyến khích thường quy vì sự căng của trực tràng và hậu quả là sự chèn ép của các mô quanh trực tràng có thể cản trở việc đánh giá chính xác khoảng cách giữa khối u và mạc treo trực tràng. Các bước chuẩn bị để giảm lượng khí trong lòng trực tràng có thể hữu ích để tránh các hiện tượng nhạy từ do khí gây ra trên trình tự DWI, mặc dù đây chủ yếu là một vấn đề trong đánh giá lại gia đoạn sau hóa xạ trị, lúc DWI đóng vai trò quan trọng hơn. Điều này có thể đạt được chẳng hạn bằng cách cho bệnh nhân uống thuốc xổ vi sinh hoặc một lượng nhỏ chất làm đầy trực tràng (tối đa 60 ml).
9.3. Các chuỗi xung sagittal
Các chuỗi sagittal được sử dụng để xác định vị trí của khối u và định vị chụp các chuỗi xung axial và coronal. Trường chụp phía trên (FOV) phải ở mức u nhô xương cùng và trường chụp phía dưới nên ở dưới mức ống hậu môn.
9.4. Các chuỗi xung axial
Hình ảnh axial hoặc axial chếch (oblique-axial) nên được đặt vuông góc với trục khối u để cho phép đánh giá thích hợp sự mở rộng của khối u ra ngoài thành trực tràng và khoảng cách giữa khối u và MRF.
9.5. Các chuỗi xung coronal
Các chuỗi xung coronal nên có góc song song với trục khối u, vuông góc với các hình ảnh axial.
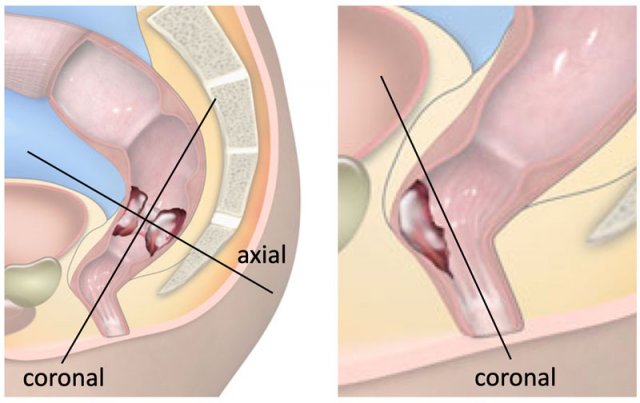 Hình 52. Trong các khối u ở thấp, gần hoặc liên quan đến ống hậu môn, các chuỗi xung coronal nên được chụp song song với ống hậu môn hoặc một mặt phẳng bổ sung song song với ống hậu môn nên được thêm vào quy trình để đánh giá đúng xem khối u có xâm lấn cơ thắt hậu môn hay không và ở mức độ nào (hình bên phải).
Hình 52. Trong các khối u ở thấp, gần hoặc liên quan đến ống hậu môn, các chuỗi xung coronal nên được chụp song song với ống hậu môn hoặc một mặt phẳng bổ sung song song với ống hậu môn nên được thêm vào quy trình để đánh giá đúng xem khối u có xâm lấn cơ thắt hậu môn hay không và ở mức độ nào (hình bên phải).
Ví dụ cho thấy tác động của góc chuỗi xung
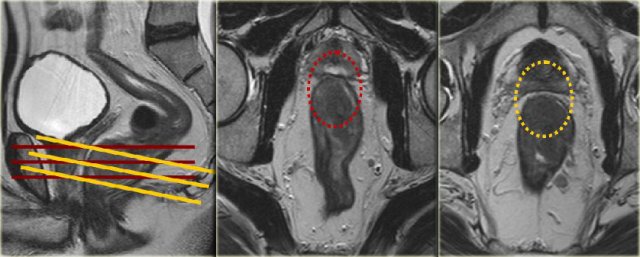 Hình 53. Ví dụ về tạo góc không đúng cách. Trong hình ảnh giữa, hình axial không vuông góc với trục khối u trực tràng thấp; điều này dẫn đến đánh giá sai là MRF có liên quan đến phía trước (vòng tròn màu đỏ). Trong hình ảnh bên phải, hình axial được chụp chính xác vuông góc với trục khối u và rõ ràng là MRF không liên quan (vòng tròn màu vàng).
Hình 53. Ví dụ về tạo góc không đúng cách. Trong hình ảnh giữa, hình axial không vuông góc với trục khối u trực tràng thấp; điều này dẫn đến đánh giá sai là MRF có liên quan đến phía trước (vòng tròn màu đỏ). Trong hình ảnh bên phải, hình axial được chụp chính xác vuông góc với trục khối u và rõ ràng là MRF không liên quan (vòng tròn màu vàng).
9.6. T2W
Protocol MRI trực tràng thường quy nên bao gồm các chuỗi T2W 2D có độ phân giải cao (high resolution 2D T2-weighted sequences) trong nhiều mặt phẳng với độ dày lát cắt ≤3mm. Mặc dù những tiến bộ kỹ thuật gần đây đã cải thiện chất lượng của các chuỗi T2W 3D, nhưng chúng vẫn chưa được sử dụng phổ biến để thay thế cho các chuỗi T2W 2D. Yêu cầu về độ phân giải mặt phẳng ít được ghi rõ trong các hướng dẫn, mặc dù độ phân giải 0.6×0.6mm hoặc nhỏ hơn thường được khuyến nghị.
9.7. DWI
Chụp thường quy nên bao gồm một chuỗi xung DWI. Hình ảnh DWI có thể hữu ích để phát hiện khối u và hạch bạch huyết trong đánh giá ban đầu và đặc biệt hữu ích cho việc đánh giá lại khối u sau khi điều trị bổ trợ. Protocol DWI nên bao gồm ít nhất một giá trị b cao ≥ 800 s/mm2. Bản đồ ADC nên được tính toán từ DWI để nghiên cứu trực quan cùng với hình ảnh DWI (xem thêm phần về cạm bẫy DWI).
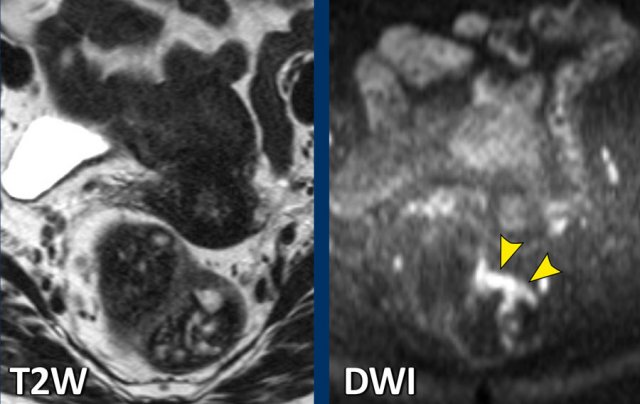 Hình 54. Ví dụ về một bệnh nhân có nhiều phân trong trực tràng. Bản thân khối u hầu như không thể nhận ra trên MRI T2W, nhưng dễ dàng xác định vị trí trên DWI.
Hình 54. Ví dụ về một bệnh nhân có nhiều phân trong trực tràng. Bản thân khối u hầu như không thể nhận ra trên MRI T2W, nhưng dễ dàng xác định vị trí trên DWI.
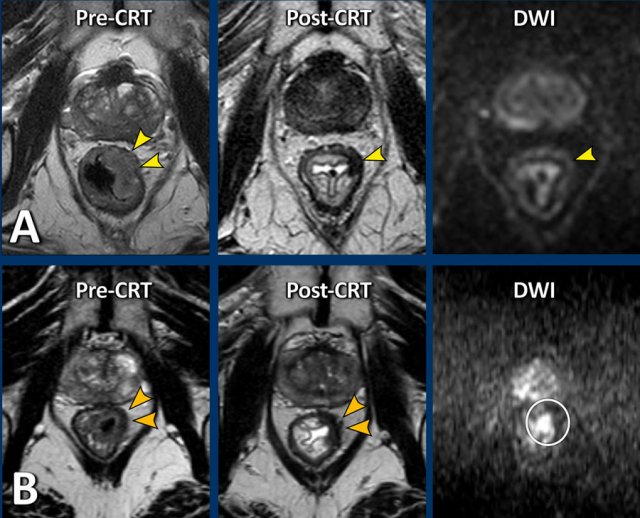 Hình 55. Đây là hai ví dụ khác về hai bệnh nhân có khối u hình bán nguyệt rất giống nhau trước và sau hóa xạ trị. Trên hình ảnh T2W sau hóa xạ trị, cả hai bệnh nhân đều cho thấy một số vùng xơ dày thành ở vùng xạ trị, nhưng không có tàn tích khối u đặc rõ ràng (đầu mũi tên màu vàng). Trên DWI, bệnh nhân A không có biểu hiện hạn chế khuếch tán dạng khối. Chỉ có một số vùng sáng của tín hiệu chất lỏng trong lòng trực tràng. Ở bệnh nhân B có sự khuếch tán hạn chế khu trú tại vị trí xơ hóa. Bệnh nhân A được xác nhận là người hoàn toàn đáp ứng khi nội soi và được lập chương trình chờ đợi đợi và quan sát thêm. Bệnh nhân B đã trải qua phẫu thuật cắt bỏ xác nhận còn sót lại khối u ypT2.
Hình 55. Đây là hai ví dụ khác về hai bệnh nhân có khối u hình bán nguyệt rất giống nhau trước và sau hóa xạ trị. Trên hình ảnh T2W sau hóa xạ trị, cả hai bệnh nhân đều cho thấy một số vùng xơ dày thành ở vùng xạ trị, nhưng không có tàn tích khối u đặc rõ ràng (đầu mũi tên màu vàng). Trên DWI, bệnh nhân A không có biểu hiện hạn chế khuếch tán dạng khối. Chỉ có một số vùng sáng của tín hiệu chất lỏng trong lòng trực tràng. Ở bệnh nhân B có sự khuếch tán hạn chế khu trú tại vị trí xơ hóa. Bệnh nhân A được xác nhận là người hoàn toàn đáp ứng khi nội soi và được lập chương trình chờ đợi đợi và quan sát thêm. Bệnh nhân B đã trải qua phẫu thuật cắt bỏ xác nhận còn sót lại khối u ypT2.
9.8. Các chuỗi xung khác
T1W: các chuỗi T1W không tiêm thuốc có thể hữu ích để giúp xác định đặc điểm của các phát hiện trùng hợp (ví dụ như tổn thương xương, u nang buồng trứng) nhưng không bắt buộc đối với việc phân giai đoạn. Các chuỗi T1W với trường nhìn mở rộng cũng có thể được sử dụng để kiểm tra tất cả các trạm hạch bạch huyết có liên quan với thời gian thu nhận tương đối ngắn.
Chuỗi xung tiêm thuốc cản quang tĩnh mạch: hình ảnh tiêm thuốc gadolinium ở chuỗi điểm vang thang từ không cải thiện độ chính xác chẩn đoán đối với việc phân giai đoạn lâm sàng và không được khuyến cáo thường quy. MRI tương phản động không được khuyến cáo thường quy cho phân giai đoạn lâm sàng.
Chuỗi xung xóa mỡ (Fat suppression): các chuỗi xóa mỡ là không cần thiết để phân giai đoạn. Hình ảnh T2W FS có thể có thêm lợi ích cho những bệnh nhân bị áp xe hoặc rò quanh hậu môn đồng thời (concommittant perianal fistulas or abscesses).
10. Phẫu thuật
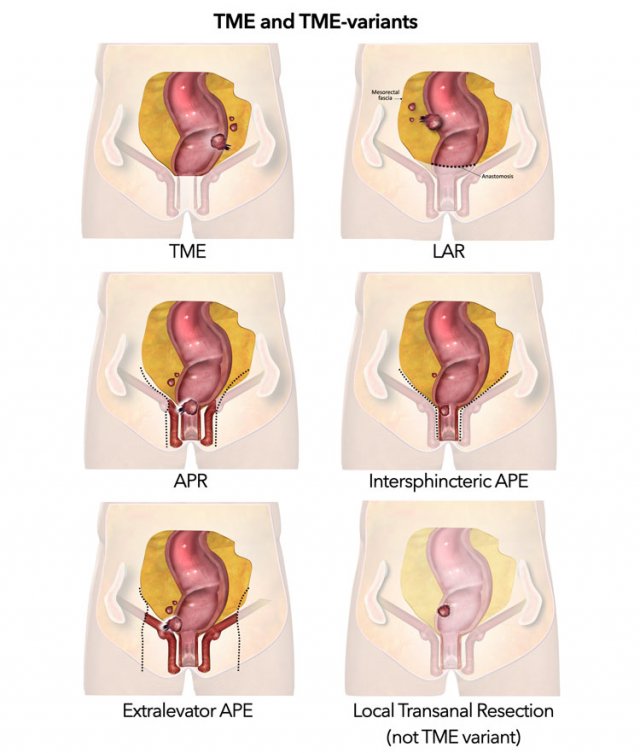
Hình 56. Minh họa các phương pháp phẫu thuật.
10.1. Phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng (Total mesorectal excision)
Quy trình phẫu thuật điều trị ung thư trực tràng tiêu chuẩn hiện nay là phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng (TME). TME là một thuật ngữ chung được sử dụng để mô tả các kỹ thuật phẫu thuật khác nhau (LAR, APR) bao gồm việc cắt bỏ toàn bộ mạc treo trực tràng dọc theo cân mạc treo trực tràng.
10.2. Phẫu thuật cắt bỏ toàn bộ mạc treo trực tràng (Low anterior resection)
Với một đường cắt trước thấp, ống hậu môn được giữ lại tại chỗ và một đường nối được tạo ra giữa trực tràng và đại tràng sigma. Do đó, cắt trước thấp thường được áp dụng cho các khối u trực tràng giữa và cao, nơi có đủ cấu trúc ranh giới phía dưới u và ống hậu môn để tạo miệng nối, phổ biến nhất là sử dụng đường nối tận bên (side-to-end anastomosis).
10.3. Cắt cụt trực tràng qua đường bụng- tầng sinh môn (Abdominoperineal resection)
Với phẫu thuật này, trực tràng và ống hậu môn được cắt bỏ và bệnh nhân được cắt đại tràng vĩnh viễn (permanent colostomy). APR được chỉ định cho các khối u trực tràng thấp với rìa nằm gần hoặc liên quan đến ống hậu môn.
10.4. Cắt cụt trực tràng qua ngả bụng tầng sinh môn trong cơ thắt (Intersphincteric abdomino perineal resection)
Đây là một biến thể đối với phẫu thuật cắt cụt trực tràng qua ngả bụng tầng sinh môn tiêu chuẩn, nơi cơ thắt ngoài được giữ lại.
10.5. Cắt cụt trực tràng qua ngả bụng tầng sinh môn ngoài cơ nâng hậu môn (Extralevator abdomino-perineal resection)
Đây là một thủ thuật mở rộng hơn bao gồm các cơ nâng hậu môn và và được chỉ định cho các khối u xâm lấn vào sàn chậu.
10.6. Cắt bỏ cục bộ
Đây là một thuật ngữ chung (umbrella term) để chỉ các kỹ thuật xâm lấn tối thiểu khác nhau (various minimally invasive techniques) để loại bỏ các khối u trực tràng qua nội soi, qua đường hậu môn. Cắt bỏ niêm mạc nội soi (endoscopic mucosal resection) và cắt bỏ dưới niêm mạc nội soi (endoscopic submucosal resection) là kỹ thuật cắt bỏ nông (superficial excision techniques) được sử dụng cho các polyp không phải ung thư (non-cancerous polyps) và các khối u T1a và T1b.
Phẫu thuật xâm lấn tối thiểu qua hậu môn (transanal minimally invasive surgery) hoặc vi phẫu nội soi qua hậu môn (transanal endoscopic microsurgery; một kỹ thuật rất tương tự nhưng cũ hơn) là phương pháp cắt bỏ bằng nội soi một khu vực thành ruột (bao gồm tất cả các lớp thành ruột) có thể được áp dụng cho các khối u T1 (và một số T2 nhỏ).
10.7. Bảo tồn nội tạng (Organ-preservation)
Ngày càng có xu hướng xem xét các lựa chọn thay thế điều trị khối u trực tràng bằng các kỹ thuật xâm lấn tối thiểu hoặc không phẫu thuật đối với các khối u cho thấy đáp ứng hoàn toàn hoặc gần hoàn toàn sau khi điều trị bổ trợ.
Những lựa chọn thay thế này bao gồm chiến lược theo dõi và chờ đợi (watch-and-wait strategy), trong đó những bệnh nhân có đáp ứng lâm sàng hoàn toàn sau khi điều trị bổ trợ được hoãn phẫu thuật và được theo dõi chặt chẽ, và kỹ thuật cắt bỏ cục bộ hoặc xạ trị cục bộ cho những tàn tích khối u nhỏ được thực hiện.
Những phát triển này đã thúc đẩy nhu cầu đánh giá hình ảnh học càng chính xác hơn sau khi điều trị bổ trợ và MRI kết hợp với nội soi và khám lâm sàng đóng một vai trò quan trọng trong việc lựa chọn và theo dõi những bệnh nhân này.
11. Nguồn
https://radiologyassistant.nl/abdomen/rectum/rectal-cancer-mr-staging-1